
Foto: verskaf
Op die periodieke tabel word al die verskillende elemente aangetoon. Elkeen van hierdie elemente het sy eie eienskappe. ’n Atoom is die kleinste deeltjie van ’n element wat nog steeds die eienskappe van daardie element toon. Atome kan aan mekaar bind om molekules te vorm. Wanneer meer as een van dieselfde atome aan mekaar bind, het die molekule nog steeds dieselfde eienskappe as die element. Atome van verskillende elemente kan ook aan mekaar bind om molekules met nuwe eienskappe te vorm.
Molekules kan met mekaar reageer om produkte met ander chemiese eienskappe te vorm. Dit word ’n chemiese reaksie genoem. In ’n chemiese reaksie word die stowwe wat met mekaar reageer, die reaktante genoem, terwyl die stowwe wat geproduseer word, die produkte genoem word. Die atome van die reaktante word herrangskik om produkte te vorm wat ander eienskappe het as die reaktante. Tydens die chemiese reaksie breek die verbindings wat die reaktante se atome bymekaar hou, en word nuwe verbindings gevorm wat die atome van die produkte nou weer aan mekaar hou.
Chemiese reaksies kan voorgestel word met modelle, woordvergelykings of chemiese vergelykings. Chemiese vergelykings is die formule waarvolgens die reaktante verbind om die produk te vorm. Chemiese vergelykings maak gebruik van simbole om die verskillende aspekte van die vergelyking aan te dui. Die mees algemeen bekende chemiese vergelykings is die vorming van koolstofdioksied (CO2) en die vorming van water (H2O):
C + O2 → CO2
2H2 + O2 → 2H2O
Die onderskrif getalle dui op die hoeveelheid atome van ’n element wat in die formule voorkom. Jy kan nooit aan die onderskrif getalle in ’n chemiese vergelyking verander nie.
Die getalle aan die voorkant van die molekules dui die hoeveelheid van die molekules wat nodig is om die chemiese vergelyking te laat balanseer aan. Dit dui dan ook die verhouding waarin die molekules met mekaar reageer aan. Dit word die koëffisiënt genoem.
Dus, om een koolstofdioksiedmolekule (CO2) te vorm, bind een koolstofatoom (C) met een suurstofmolekule wat uit twee atome bestaan (O2).

Koolstof + suurstof → koolstofdioksied
Om twee waterstofmolekules (2H2O) te vorm, bind twee watermolekules wat elk uit twee atome bestaan (2H2), met een suurstofmolekule wat uit twee atome bestaan (O2). Die verhouding van waterstof tot suurstof (H:O) is 2:1.
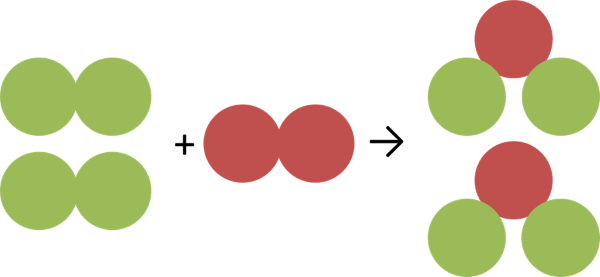
Waterstof + suurstof → water
Geen atome gaan verlore in ’n gebalanseerde chemiese vergelyking nie. Hulle word net herrangskik.
As jy na die skets kyk, sal jy sien dat daar vier groen en twee rooi atome links van die pyl is. Regs van die pyl is daar steeds vier groen en twee rooi atome. Hulle sit net op ander plekke. Dieselfde is waar vir die koolstofdioksied vergelyking. Links van die pyl is daar een blou en twee rooi atome. Regs van die pyl is daar steeds een blou en twee rooi atome. Hulle is nou net aan mekaar verbind.
Die hoeveelheid atome van elke tipe element moet dieselfde wees links en regs van die pyl om die vergelyking gebalanseerd te maak. Omdat geen atome verlore gaan in ’n chemiese reaksie nie, moet ons chemiese vergelykings balanseer.
Die volgende reaksie dui aan hoe roes vorm:
4Fe + 3O2 → 2Fe2O3
Let op dat daar vier ysteratome (4Fe) links van die pyl is. Regs van die pyl is daar twee ystermolekules wat elk uit twee atome bestaan (2Fe2O3). 2 x 2 = 4. Daar is dus steeds vier ysteratome regs van die pyl. Daar is ook drie suurstofmolekules wat elk uit twee atome bestaan (3O2) links van die pyl. Daar is dus 3 x 2 = 6 suurstofatome links van die pyl. Regs van die pyl is daar twee molekules wat elk drie suurstofatome bevat (2 Fe2O3). Daar is dus steeds 2 x 3 = 6 suurstofatome regs van die pyl.
Die volgende chemiese reaksie dui die vorming van koperoksied aan:
2Cu + O2 → 2CuO
Hierdie chemiese vergelyking se woordvergelyking lyk soos volg:
Koper + suurstof → koperoksied
Sommige verbindings het algemene name, soos water (H2O) of ammoniak (NH3). Die meeste verbindings word egter beskryf volgens die elemente waaruit hulle bestaan. Koolstofmonoksied (CO), koolstofdioksied (CO2) en swaeltrioksied (SO3) is voorbeelde van sulke name. In hierdie verbindings verwys monoksied na die feit dat daar net een suurstofatoom in die verbinding is. Dioksied dui aan dat daar twee suurstofatome in die verbinding is en trioksied dui aan dat daar drie suurstofatome in die verbinding is.
Chemiese reaksies is oral rondom ons waarneembaar. Ons is net nie altyd daarvan bewus nie. Ook in die natuur gebeur daar gereeld allerhande chemiese reaksies.
Kom ons kyk hoe die bombardierkewer van chemiese reaksies gebruik maak.
Die bombardierkewer het ’n besonderse manier van selfverdediging. Hy spuit sy vyande met ’n kokend-warm, giftige stoom. Om dié spuitstof te vorm, gebeur daar ’n interessante chemiese reaksie binne-in ’n ontbrandingskamer in die kewer se liggaam. Voor die ontbrandingskamer is daar twee aparte opgaartenke. ’n Klep keer dat die inhoud van die twee opgaartenke meng. Wanneer die kewer bedreig voel, maak die klep oop. Die inhoud van die tenke vloei dan na die ontbrandingskamer. Hier gebeur die volgende chemiese reaksie:
Hidrokinoon + waterstofperoksied → benzokinoon + water
Die chemiese vergelyking lyk so:
C6H4(OH)2 + H2O2 → C6H4O2 + 2H2O
Een van die kewer se opgaartenke bevat hidrokinoon (C6H4(OH)2) en die ander tenk bevat waterstofperoksied (H2O2).
Waterstofperoksied (H2O2) is ’n onstabiele molekuul wat maklik afbreek tot water (H2O). Dit veroorsaak dat die druk in die ontbrandingskamer toeneem. Die hidrokinoonmolekules (C6H4(OH)2) verander na benzokinoon (C6H4O2). Benzokinoon (C6H4O2) is ’n geel kristal wat sleg ruik en toksies is. Benzokinoon (C6H4O2) kan jou vel brand en jou oë en asemhalingsisteem irriteer. Dit is net so gevaarlik vir insekte en selfs ook ander diere soos paddas en muishonde. Die chemiese reaksie laat baie hitte vry. Wanneer die temperatuur van benzokinoon (C6H4O2) naby aan 115°C kom, verander dit in ’n giftige gas.
Die hele reaksie laat dus hitte, benzokinoongas (C6H4O2) en water (H2O) onder hoë druk vry. Mens kan dit sien as ’n stomende vloeistof wat met ’n klapgeluid uitgespuit word. Dit is net soos ’n mini-ontploffing!
Bombardierkewers is baie meer algemeen as wat ’n mens dink. Hulle kom op elke kontinent behalwe Antarktika voor. Al wat hulle nodig het, is ’n klam plekkie om hulle eiers te lê. Bombardierkewers is vleisvretend en kom in die nag uit om ander insekte te soek wat hulle kan eet.

Bombardierkewers kan hul vyande met ’n gifitge stoom spuit. (Foto: verskaf)
In hierdie foto is ’n stukkie vleis, wat as vis-aas gebruik is, op die sand gelos. Na donker het ’n hele paar bombardierkewers hieraan begin smul.
Chemiese reaksies gebeur oral rondom ons, en elke vergelyking is gebalanseerd. Atome gaan nie rondom ons verlore nie, maar verander eerder van posisie om nuwe molekules te vorm. Soms word hitte vrygelaat deur die reaksie en soms benodig ’n reaksie hitte om te kan plaasvind. Ons mense maak gebruik van chemiese reaksies om metale uit rou materiale te onttrek. Chemiese reaksies word gebruik om kos te preserveer. Chemiese reaksies vind plaas wanneer ’n brandstof, soos petrol, verbrand word. Chemiese reaksies kom oral rondom ons voor, selfs al is ons gewoonlik nie eens bewus daarvan nie.
Lees ook:
Lewenswetenskappe: Sure en basisse, miere en termiete – het hulle iets gemeen?
Graad 8: Lewenswetenskappe – aanpassings vir oorlewing in die droë Karoo
Lewenswetenskappe: Predator of prooi? Die mierleeu se plek in die ekosisteem
Lewenswetenskappe: Chlorofil, fotosintese en blaarmyners – hoe om groen te bly

