|
||||||
Opsomming
Perlemoenboerdery is een van Suid-Afrika se belangrikste akwakultuurbedrywe. Van die grootste probleme in hierdie bedryf is die stadige groeitempo van die perlemoen en ekonomiese verliese as gevolg van siektes. Daar word derhalwe swaar gesteun op die gebruik van antibiotika vir die beheer en behandeling van bakteriële infeksies in akwakultuurspesies. As gevolg van die ontwikkeling van antibiotikaweerstandigheid in bakterieë en die betreklik maklike verspreiding daarvan in akwatiese omgewings, word die gebruik van antibiotika bevraagteken. ’n Alternatief vir die gebruik van antibiotika is probiotika, ’n lewende mikrobiese aanvulling wat ’n positiewe effek op die gasheer het, en wat die mikrobiese gemeenskappe wat met die gasheer en die onmiddellike omgewing geassosieer word, verander. Die doel van hierdie studie was die isolering en identifisering van bakterieë in die spysverteringsverteringskanaal (SVK) van Suid-Afrikaanse perlemoen, Haliotis midae. Die isolate is oorweeg as ’n potensiële probiotikum gebaseer op bestaande literatuur.
Perlemoen is vanaf Abagold-perlemoenplaas (Hermanus, Suid-Afrika) verkry. Die SVK van elke perlemoen is asepties verwyder, fyn gemaal en op drie verskillende groeimedia uitgeplaat. Die plate is vir 3–7 dae by 20°C geïnkubeer. Verteenwoordigende suiwer isolate is op grond van hul morfologiese eienskappe, Gramkleuring, oksidase- en katalasetoetse vir DNS-isolasie gekies. Die 16S ribosomale RNS-gedeelte van die geselekteerde isolate is deur ’n polimerasiekettingreaksie (PKR) vermeerder en hierdie produkte is verder gesny deur van die ensiem RsaI gebruik te maak. Isolate is volgens die beperkingsensiemprofiele wat verkry is, gegroepeer, en verteenwoordigers van elke groep is met behulp van DNS-volgordebepaling vir identifikasie gekies. Spesies van vyf verskillende genera is geïdentifiseer. Hierdie genera sluit in Grampositiewe spesies van die niebeweeglike, staafvormige Corynebacterium en kokkusvormige Staphylococcus. Gramnegatiewe isolate wat geïsoleer is, sluit spesies van die staafvormige Vibrio-genus in, wat algemeen in akwatiese omgewings gevind word, asook die naverwante Photobacterium. Paracoccus-spesies wat bekend is vir die produksie van die antioksidant astasantien is ook geïsoleer. Laasgenoemde isolaat toon potensiaal om gebruik te kan word as ’n moontlike probiotikum as gevolg van die astasantienproduksie.
Trefwoorde: akwakultuur; antibiotikum; bakterium; isolaat; probiotikum
Abstract
Partial description of bacteria in the gastrointestinal track of Haliotis midae, with the focus on potential probiotics
The ocean’s fish resources are declining mainly because of irresponsible exploitation. Fish is a vital source of protein for humans, and growing world populations are threatening the sustainability of commercial fisheries. This has led to the rapid growth of aquaculture worldwide. In South Africa, aquaculture of both fresh and marine species is expanding and is now practised in all nine provinces of the country.
One of the major problems in aquaculture is financial loss as a result of disease. Viruses, bacteria, fungi and parasites are known to infect fish, with bacteria causing the majority of diseases. One of the largest groups of disease-causing bacteria in aquaculture comes from the family Vibrionaceae. The genus Vibrio includes more than 30 species and many are pathogenic. Major abalone pathogens from this genus include V. splendidus and V. harveyi. Disease outbreaks usually occur during the summer abalone spawning period, when there is a sharp increase in water temperature. During this period the energy reserves of the abalone are limited and their immune systems are relatively suppressed. Other stress-related factors, such as handling or poor water quality, may also contribute to disease outbreaks.
Antibiotics have commonly been used to control diseases; however, due to their negative impact on the environment the use of these agents is being questioned. One of the major concerns regarding dispersing antibiotics in aquatic environments is the development of antibiotic resistance in bacteria. Studies found that more than 70% of bacteria found in aquatic environments are resistant to at least one antibiotic. Furthermore, many bacteria have been shown to have resistance to multiple antibiotics. A major concern of antibiotic-resistant bacteria in aquatic environments is the transfer of resistance between aquatic and terrestrial environments. The spread of antibiotic resistance through aquacultural activities, therefore, holds a significant risk to human health.
This has led to the search for probiotics as an alternative way to control bacterial diseases in aquaculture. Probiotics used in aquatic environments can be defined as live microbial supplements which have beneficial effects on the host by altering the microbial communities associated with the host and the immediate environment. The use of probiotics in terrestrial vertebrates such as pigs, chickens and humans have been studied extensively. Probiotics for terrestrial animals have been applied in aquaculture with varied success. Studies found that probiotics isolated from the environments in which they will be applied, such as aquatic environments, yield better results. In order to obtain potential probiotics for aquaculture, candidate bacteria should ideally be isolated from the GIT of aquatic species. Research on the use of probiotics in aquaculture is growing rapidly and is showing promising possibilities.
Probiotics have a variety of mechanisms of action. These bacteria can eliminate or reduce colonisation of the host by pathogenic organisms through the secretion of antagonistic compounds. These compounds can be defined as chemical substances produced by microorganisms that inhibit or are toxic towards other microorganisms in the surrounding environment. Antagonistic compounds include the production of secondary metabolites such as antibiotics and bacteriocins, which are produced by some bacteria to kill or inhibit the growth of surrounding bacteria, fungi and viruses. Probiotic bacteria can produce a variety of compounds that can be beneficial to the host, such as enzymes, vitamins, proteins, short-chain fatty acids and carotenoids. Probiotic bacteria can also enhance the immune response of the host. Certain bacterial compounds are known to act as immunostimulants. These compounds elicit different host responses, namely phagocytic activity and lysozyme production. Phagocytic activity plays an important role in antibacterial defences. Before antibodies are produced, phagocytic activity serves as an early activator of the inflammatory response.
The aim of this study was to isolate and identify bacteria in the gastrointestinal track of the South African abalone Haliotis midae and to evaluate the isolates' potential as a probiotic based on existing literature. Abalone were collected from Abagold farm (Hermanus, South Africa). The gut of each abalone was removed under aseptic conditions and transferred into sterile saline solution (0,9% NaCl) containing acid-washed glass beads (Sigma, South Africa). Each gut sample was homogenised and plated out on to three different media, Tryptone Soya agar (Casein enzymic hydrolysate 17g/l, papaic digest of soya bean meal 3g/l, D-Glucose 2,5g/l, bile salts mixture 1,5g/l, dipotassium hydrogen phosphate 4g/l, sodium chloride 5g/l and agar 12g/l), De Man, Rogosa and Sharpe agar (Universal peptone 10g/l, meat extract 5g/l, yeast extract 5g/l, D(+)-Glucose 20g/l, dipotassium hydrogen phosphate 2g/l, diammonium hydrogen citrate 2g/l, sodium acetate 5g/l, magnesium sulfate 0,1g/l, manganous sulfate 0,05g/l and agar 12g/l] and Zobell agar (Polypeptone 5g/l, yeast extract 1g/l and agar 12g/l). Random colonies were picked from the growth on different plates and streaked out in order to obtain pure cultures. Based on Gram stains, catalase and oxidase tests that were performed, representative strains were selected for DNA extractions. After successful DNA extractions the 16S ribosomal RNA region was amplified by PCR and these products were digested with RsaI (Fermentas Life Science, division of Thermo Fisher Scientific, Massachusetts, USA). Based on the patterns obtained from restriction enzyme profiles, representative isolates from each pattern were selected for DNA sequencing for identification.
Nine different bacterial species were isolated and identified as Corynebacterium variabilei, Staphylococcus carnosus, Staphylococcus equorum, Staphylococcus cohniii, Vibrio aestuarianus, Vibrio nigripulchritudo, Vibrio cyclitrophicus, Photobacterium leiognathi and Paracoccus marcusii. One of these isolates, P. marcusii, is able to produce the carotenoid astaxanthin, an orange-red pigment with a very high antioxidant activity. As a result of the production of this pigment, P. marcusii shows promising probiotic properties due to the high antioxidant activity that enhances essential biological functions of fish such as increasing the defence potential against oxidative stress and enhancing sexual maturity. This bacterial isolate also shows potential to be used as a pigmentation source due to the production of astaxanthin. Certain fish species, such as salmonids, red sea bream, trout, lobster and shrimp are unable to synthesise carotenoids and have to obtain the pigments from their natural diets. However, under aquacultural conditions these fish species do not come into contact with natural pigments and this results in dark grey meat, which is unappealing to consumers. It is, therefore, important to include these carotenoids in the diet of certain aquaculture fish species such as salmonids, red sea bream, trout, lobster and shrimp. To conclude, Paracoccus marcusii shows possible probiotic properties and industrial applications based on the production of the astaxanthin pigment. Further in vivo studies need to be conducted in order to determine if P. marcusii can be used as an effective aquacultural feed additive.
Keywords: aquaculture, antibiotic, probiotic, bacterium, isolate
1. Inleiding
Vis is ’n belangrike bron van proteïene vir mense regoor die wêreld, met sowat een miljard mense wat vis as hoofproteïenbron gebruik (Tidwell en Allan 2001). As gevolg van die toenemende wêreldbevolking word die volhoubaarheid van kommersiële visserye egter bedreig (Garcia en Rosenberg 2010; Sargent 1997). Om hierdie redes is daar dus wêreldwyd ’n drastiese toename in die akwakultuurbedryf. Akwakultuur kan gedefinieer word as die insluiting van waterlewende diere soos visse, skulpdiere ens. in ’n beskermende sisteem onder optimale toestande (Naylor e.a. 2000). Die toename in akwakultuur word nie net veroorsaak deur ’n vermeerdering in die vraag na voedsel nie, maar help ook met die bewaring van akwatiese biodiversiteit en natuurlike ekosisteme (Tidwell en Allan 2001). Hierdie bedryf hou ook verskeie ekonomiese voordele in, onder andere werkskepping en buitelandse valuta (Balcázar e.a. 2007; Bostock e.a. 2010; Wang e.a. 2008).
In Suid-Afrika is daar ook ’n toename in die akwakultuurbedryf van beide varswater- en mariene spesies (Garcia en Rosenberg 2010). Een van die land se belangrikste akwakultuurbedrywe is perlemoenboerdery (Macey en Coyne 2005; Ten Doeschate en Coyne 2008). Van die grootste probleme in akwakultuur, en spesifiek ook in perlemoenboerdery, is die stadige groeitempo van perlemoen en geldelike verliese as gevolg van siektes. Onder akwakultuur groei perlemoen vinniger as in die natuur, maar het nog steeds vier tot vyf jaar nodig om die lewensiklus te voltooi en om markgrootte te bereik (Macey en Coyne 2005; Ten Doeschate en Coyne 2008). In hierdie vier tot vyf jaar is die perlemoen vatbaar vir verskeie siektes wat deur virusse, swamme en parasiete veroorsaak kan word, maar bakteriële siektes is die algemeenste (Boudinot e.a. 1998; Brunt en Austin 2005; Muraosa e.a. 2009; Rimstad 2011). Antibiotika word algemeen gebruik in die beheer van bakteriële siektes en word gewoonlik as deel van die visvoer toegedien (Cabello 2006; Heuer e.a. 2009; Hirsch e.a. 1999). ’n Groot persentasie van hierdie antibiotika word egter nie deur die vis opgeneem nie, maar saam met die ontlasting uitgeskei (Rigos en Troisi 2005). Die ontlasting en onverteerde voer wat die antibiotika bevat, beland in die sediment van damme en kan dan deur strome na ander dele van die akwatiese omgewing versprei word (Cabello 2006). Een van die grootste bekommernisse is die ontwikkeling van antibiotikaweerstandigheid in veral patogeniese bakterieë (Farzanfar 2006). Studies het bevind dat meer as 70% van akwatiese bakterieë teen minstens een antibiotikum weerstandbiedend is, en dat die meerderheid van hierdie bakterieë teen meer as een antibiotikum weerstand kan bied (Hirsch e.a. 1999). Antibiotikumweerstandbiedende gene kan tussen akwatiese en terrestriële bakterieë uitgeruil word en hou ’n groot gevaar vir menslike gesondheid in (Heuer e.a. 2009). Die gebruik van antibiotika, veral in akwatiese omgewings, word dus as gevolg van verskeie negatiewe implikasies vir die omgewing en menslike gesondheid bevraagteken, en in sommige lande selfs verbied (Cabello 2006; Guglielmetti e.a. 2009; Hirsch e.a. 1999). As ’n alternatief vir die gebruik van antibiotika word probiotika al hoe meer algemeen vir die behandeling en voorkoming van bakteriële siektes gebruik.
Probiotika wat in akwatiese omgewings toegedien word, kan gedefinieer word as ’n lewende mikrobiese aanvulling wat ’n positiewe effek op die gasheer het deur die mikrobiese gemeenskappe wat met die gasheer en die onmiddellike omgewing geassosieer word te verander (Verschuere e.a. 2000). Daar is reeds baie navorsing gedoen oor die gebruik van probiotika vir landlewende diere soos varke, hoenders en mense. Probiotika wat vir landlewende diere gebruik word, is al in akwakultuur gebruik, maar lewer nie altyd optimale resultate nie (Venkat e.a. 2004). Studies het getoon dat probiotika wat geïsoleer is vanuit die gasheer waar dit toegedien word, baie beter resultate lewer (Burr en Gatlin 2005; Erasmus e.a. 1997; Macey en Coyne 2006; Vine e.a. 2004). Hierdie stelling word gestaaf deur onder andere twee studies wat op perlemoen gedoen is. Probiotiese stamme wat vanuit die SVK van H. midae geïsoleer is, was in staat om die groeitempo en weerstand teen siektes te verhoog. Hierdie stamme was ook in staat om die SVK van die perlemoen te koloniseer (Macey en Coyne 2006). In ’n ander studie is daar bewys dat bakterieë wat in die SVK van die perlemoen voorkom, komplekse polisakkarides kan verteer. Die hoofvoedingsbron van perlemoen is alge wat uit komplekse polisakkarides soos sellulose en alginaat bestaan. Die afbraak van hierdie polisakkarides deur bakterieë help dus met vertering en opname van nutriënte wat die groeitempo van die perlemoen kan bevoordeel (Erasmus e.a. 1997).
Probiotika verbeter die gesondheid van die gasheer deur verskeie meganismes. Hierdie meganismes sluit onder andere in: die kompetisie met patogeniese bakterieë, produksie van voordelige chemiese verbindings, verbeterde immuniteit en antivirale aktiwiteit (Balcázar e.a. 2007; Cleveland e.a. 2001; Rengpipat e.a. 1998; Verschuere e.a. 2000).
1.1 Kompetisie met patogeniese bakterieë
Probiotiese bakterieë kan deur die produksie van antagonistiese komponente die kolonisering van patogene verminder of selfs voorkom (Balcázar e.a. 2007; Verschuere e.a. 2000). Hierdie antagonistiese komponente is chemiese verbindings wat inhiberend of selfs toksies is vir ander mikrobes in die onmiddellike omgewing. Voorbeelde van hierdie verbindings sluit in sekondêre metaboliete soos antibiotika en bakteriosiene (Cleveland e.a. 2001; Kümmerer, 2009).
Die produksie van antagonistiese komponente is nie die enigste manier waarop probiotiese bakterieë met patogene kompeteer nie. Alternatiewe maniere sluit beter groei-eienskappe soos ’n korter sloerfase en verdubbelingstyd in (Vine e.a. 2004). Probiotika kompeteer ook met die patogene vir ’n aanhegtingsplek in die gasheer, sodat selle in die SVK kan verdeel en ook antagonistiese verbindings produseer (Verschuere e.a. 2000). Kompetisie vir voedingstowwe vind ook algemeen tussen patogene en probiotiese bakterieë plaas en speel ’n belangrike rol in die mikrobiese samestelling van die SVK (Vine e.a. 2006).
Daar is reeds verskeie studies gedoen oor die inhiberende effek van verskillende probiotiese bakterieë op akwatiese patogene (Austin e.a. 1995; Austin en Billaud 1990; Harzevili e.a. 1998; Rengpipat e.a. 1998; Ten Doeschate en Coyne 2008). Daar is voorheen bewys dat Pseudomonas fluoescens (AH2) in staat is om ’n algemene forelpatogeen, Vibrio anguillarum, te inhibeer en so ook die vissterftes te verlaag (Ten Doeschate en Coyne 2008). In ’n soortgelyke studie is daar bewys dat ook Lactococcus lactis in staat is om die patogeen Vibrio anguillarum te inhibeer (Harzevili e.a. 1998). Die probiotiese Bacillus S11 wat van swart tiergarnale geïsoleer is, verlaag sterftes as gevolg van Vibrio harveyi in geïnfekteerde garnale viervoudig (Rengpipat e.a. 1998). Ander probiotiese bakterieë sluit Planococcus in wat die Atlantiese salmpatogeen Serratia liquefaciens inhibeer (Austin en Billaud 1990), asook Vibrio alginolyticus, wat die groei van Aeromonas salmonicida, Vibrio anguillarum en V. ordalii kan inhibeer (Austin e.a. 1995).
1.2 Produksie van voordelige chemiese verbindings
Probiotiese bakterieë produseer ’n verskeidenheid verbindings, insluitend ekstrasellulêre ensieme, vitamiene en karotenoïede, wat voordelig vir die gasheer kan wees. Ensieme kan die gasheer moontlik met die vertering van voedsel help (Wang 2007). Algemene ensieme wat deur die bakterieë geproduseer word, sluit sellulase, protease, lipase en chitinase in (Harris 1993). Sommige probiotiese bakterieë kan ook vitamiene soos vitamien K (Poston 1964) en B12 as sekondêre produkte produseer, wat voordele vir die gasheer kan inhou (Baya e.a. 1981; Croft e.a. 2005; Merchie e.a. 1997; Poston, 1964; Sugita e.a. 1991; Vine e.a. 2006). Sommige bakterieë is in staat om karotenoïede as sekondêre metaboliete te produseer. Daar bestaan meer as 600 karotenoïede wat in verskillende groepe ingedeel kan word. Twee van die belangrikste groepe sluit in karoteen, wat die antioksidant β-karoteen bevat, en xantofiel, wat die pigment en antioksidant astasantien bevat (Figuur 1) (Higuera-Ciapara e.a. 2006; Martin e.a. 2008; Tapiero e.a. 2004). 'n Voorbeeld van waar bakterieë in staat is om ’n karatenoïed as ’n sekondêre metaboliet te produseer, is die produksie van astasantien deur sekere Paracoccus spesies (Bjerkeng e.a. 1999; Choubert e.a. 2009; Gomes e.a. 2002).
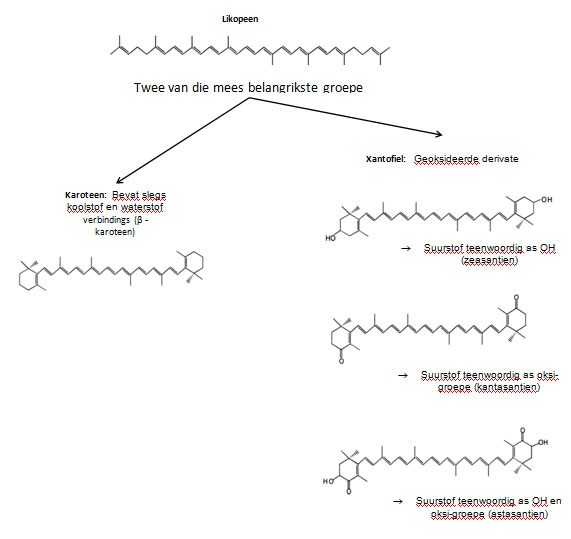
Figuur 1. Vloeidiagram van die twee belangrikste karatenoïedgroepe, karoteen en xantofiel (aangepas van Higuera-Ciapara e.a. 2006; Martin et al., 2008; Tapiero et al., 2004)
1.3 Verbeterde immuniteit
Die vermoë van probiotiese bakterieë om die immuniteit van diere, mense en visse te verbeter, is al baie bestudeer. Sommige verbindings wat deur probiotiese bakterieë geproduseer word, stimuleer die gasheer se immuunstelsel (Verschuere e.a. 2000). Hierdie immuunstelselreaksies kan onder andere fagositiese aktiwiteit en die produksie van lisosiem insluit. Fagositiese aktiwiteit speel ’n belangrike rol in antibakteriële beskerming in die gasheer en dien as ’n vroeë aktiveerder van die inflammatoriese reaksie nog voor die produksie van teenliggaampies plaasvind. Voorbeelde van probiotiese bakterieë wat die vermoë het om die fagositiese selle in die gasheer te aktiveer, is Lactobacillus acidophilus, L. rhamnosus en L. lactis (Nayak 2010; Panigrahi e.a. 2004; Ringø 1999).
Lisosiem, ook ’n immuunstimuleerder, is ’n belangrike ensiem wat ’n groot rol speel in die beskerming teen siektes in visse (Nayak 2010). Die ensiem hidroliseer N-asetielmuramiensuur en N-asetielglukosamien, die boublokke van peptidoglikaan in die selwande van bakterieë (Balcázar e.a. 2007). Daar is bevind dat die probiotiese spesies Carnobacterium maltaromaticum, C. divergens en L. rhamnosus in staat was om die lisosiemaktiwiteit in reënboogforel te verhoog (Kim en Austin 2006). In bruinforel het die probiotiese bakterieë Lactococcus lactis en Leuconostoc mesenteroides ook ’n verhoging in die lisosiemvlakke getoon (Balcázar e.a. 2007). Hierdie verhoogde lisosiemvlakke speel ’n belangrike rol in die vis se beskerming teen bakteriese patogene (Grinde e.a. 1988).
1.4 Antivirale effekte
Virale siektes is ’n groot probleem in akwakultuur. Studies het bewys dat virusse deur ekstrasellulêre agente van probiotiese bakterieë geïnaktiveer word, maar die meganismes is nog onduidelik (Wang e.a. 2008). Bakteriespesies soos Vibrio sp., Pseudomonas sp. en Aeromonas sp. wat vanuit ’n salmbroeiplaas geïsoleer is, het antivirale effekte teen die IHNV (hematopoietiese nekrosevirus) getoon (Kamei e.a. 1988). Moraxella toon ook antivirale effekte teen die poliovirus (Balcázar e.a. 2007). Stamme van Vibrio, geïsoleer vanuit akwakultuurgarnale, het ook antivirale aktiwiteit teenoor die Oncorhynchus masou-virusse IHNV en OMV getoon en dit is toegeskryf aan antivirale verbindings wat deur die bakterieë geproduseer is (Direkbusarakom e.a. 1998).
1.5 Ontwikkeling van nuwe probiotikum
In die ontwikkeling van ’n nuwe probiotikum word ’n reeks stappe gevolg (Figuur 2). Eers word potensiële bakterieë vanuit die omgewing waar die probiotikum toegedien gaan word, geïsoleer. Die isolate word dan geïdentifiseer en in vitro-studies bepaal of die isolate enige potensiaal het om as ’n probiotikum gebruik te kan word. Suksesvolle kandidate word dan deur ’n proef geëvalueer. Indien ’n isolaat ’n probiotiese effek op die akwakultuurspesies getoon het, word daar bepaal of dit koste-effektief sal wees om die isolaat op groot skaal te produseer (Verschuere e.a. 2000; Vine e.a. 2006).

Figuur 2. Stappe vir die isolering van nuwe probiotiese bakterieë. Van die isolering van die bakterieë tot die bepaling van die koste-effektiwiteit vir grootskaalse produksie (aangepas vanaf Verschuere e.a. 2000; Vine e.a. 2006)
Uit die literatuur is dit dus duidelik dat die akwakultuurbedryf toenemend uitbrei en ’n belangrike rol speel in die voorsiening van proteïene vir baie mense regoor die wêreld. As gevolg van siektes tydens akwakultuurtoestande en die nadelige effek wat die gebruik van antibiotika inhou, raak die ontwikkeling en gebruik van probiotika al hoe belangriker. Die doel van hierdie studie was die isolering en identifisering van bakterieë in die spysverteringsverteringskanaal (SVK) van Suid-Afrikaanse perlemoen, Haliotis midae. Die isolate is oorweeg as potensiële probiotikum vir 'n wyer reeks akwakultuurspesies, gebaseer op bestaande literatuur.
2. Metode
2.1 Voorbereiding van perlemoenmonster
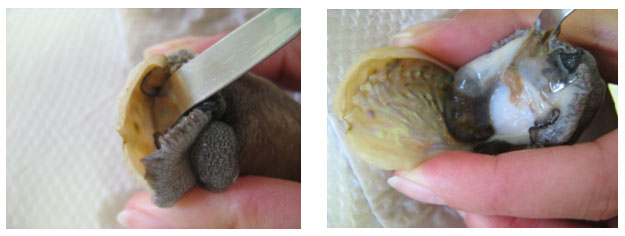
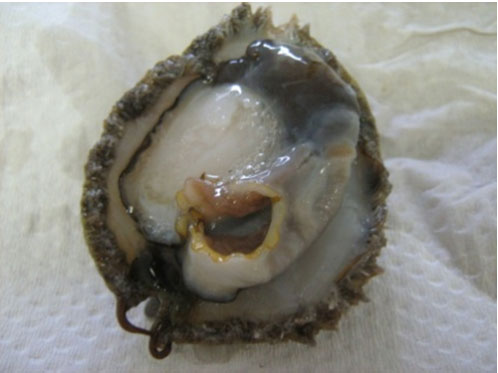
Twee groepe van tien perlemoene elk is onderskeidelik op 9 Maart en 4 Mei 2010 vanaf die Abagold-perlemoenplaas versamel. Die SVK van elke perlemoen is asepties verwyder. Elke SVK is in ’n aparte steriele houertjie met 10 ml steriele fisiologiese soutoplossing (0,9% NaCl) en suurgewaste glasballetjies (Sigma, Suid-Afrika) geplaas. Voordat die SVK’s in die steriele houertjies geplaas is, is die fekale inhoud van elke kanaal versigtig verwyder (Figuur 3a-e).
2.2 Kweek van enteriese bakterieë
Elke SVK is fyn gemaal deur dit vir 5–7 minute op ’n Vortex-2 Genie te meng (Figuur 3f). ’n Verdunningsreeks van 10–4–10–7 is van elke SVK-monster voorberei. Die verdunnings, saam met een onverdunde monster van elke SVK, is op drie verskillende mikrobiese groeimedia wat voorberei is met gefiltreerde seewater, uitgeplaat. Die media wat gebruik is, sluit Triptoon Soja agar (TSA), De Man, Rogosa en Sharpe agar (MRS) en Zobell agar in. Nadat al die monsters uitgeplaat is, is die plate vir 3–7 dae by 20°C geïnkubeer. Verskillende bakteriekolonies is ewekansig vanaf die plate gekies en uitgestreep sodat reinkulture verkry kon word. Die reinkulture is in 100 nM CaCl2 en 15% gliserol by –80°C gestoor.
2.3 Keuse van stamme vir identifikasie
Gramkleuring, katalase- en oksidasetoetse is op die reinbakteriële kulture uitgevoer en isolate is volgens fisiologiese eienskappe gegroepeer. Isolate verteenwoordigend van elke fisiologiese groep is vir verdere identifikasie gekies gekies. Die totale genoom DNS van die geselekteerde isolate is uitgehaal deur van die ZR Fungal/Bacterial DNA kitTM (Zymo Research Corp., VSA) gebruik te maak. Die teenwoordigheid van die DNS is bevestig op ’n 1% agarose-gel wat onder ultraviolet lig met etidiumbromied (EtBr) gekleur is. Daarna is die 16S ribosomale RNS-gedeelte deur ’n polimerasekettingreaksie (PKR) geamplifiseer. Bakteriële spesifieke inleiers (FORB 5’-AGAGTTTGATCCTGGCTCAG-’3 en REVB 5’-GGTTACCTTGTTACGACTT-’3) is in ’n 20 µl-reaksie gebruik. Die PKR- kondisies het bestaan uit ’n aanvanklike denaturering by 94°C vir 10 minute gevolg deur 36 siklusse van 30 sekondes elk by 94°C, 30 sekondes by 55°C en 1 minuut by 72°C. Die reaksie is voltooi deur ’n finale verlengingstap van 7 minute by 72°C, waarna die temperatuur verlaag is tot 4°C.
Figuur 3. Aseptiese verwydering van die SVK van ’n perlemoen. a. Suid-Afrikaanse perlemoen, Haliotis midae. b. en c. Verwydering van die perlemoenskulp om toegang toe die ingewande te verkry. d. Ingewande van ’n perlemoen soos van bo gesien. e. Elke SVK is in ’n aparte steriele houertjie geplaas. f. Fynmaal van ’n SVK op ’n Vortex-2 Genie.
Nadat die produkte van die PKR-reaksie op ’n 1 % agarose-gel bevestig is, is die produkte gesny deur gebruik te maak van die beperkingsensiem RsaI (Fermentas Life Science, Division of Thermo Fisher Scientific, Massachusetts, VSA). Die reaksiemengsel is saamgestel uit 10 µl van die PKR-produk, 18 µl nukleasevrye water, 2 µl 10x Buffer TangoTM (Fermentas Life Science, Division of Thermo Fisher Scientific, Massachusetts, VSA) en 1 µl RsaI en vir 8 ure by 37°C geïnkubeer. Die verteerde DNS is met behulp van ’n etidiumbromied (EtBr) bevattende 1,5% agarose-gel onder ultraviolet lig gevisualiseer. Die beperkingsensiemprofiele is gebruik om kulture vir die bepaling van DNS-volgorde te kies.
2.4 Identifisering van geïsoleerde bakterieë
DNS-volgordes van die 16S rRNS-geen van geselekteerde kulture is op ’n genetiese ontleder bepaal deur gebruik te maak van die BigDye® Terminator Kit (Applied Biosystems, Kalifornië, VSA). Die reaksiemengsels het bestaan uit 1,5 µl BigDye, 1,5 µl ½ BigDye, 5 µl nukleasevrye water, 1 µl PKR-produk en 1 µl voorganger (FORB of REVB). Vir elke isolaat is daar twee reaksiemengsels opgestel, een wat die FORB-voorganger bevat en ’n ander reaksie wat die REVB-voorganger bevat. Dit is gedoen sodat die DNS-volgordes van elke isolaat in die vorentoe en teenoorgestelde rigtings bepaal word. DNS-volgordes wat so verkry is, is vergelyk met verwante groepe wat vanaf die NCBI-databasis (National Center for Biotechnology Information) verkry is. Outomatiese belynings is uitgevoer deur gebruik te maak van CLUSTAL_X (Thompson e.a. 1997). Filogenetiese verwantskappe is deur naaste-by-boom-analiserings bepaal, deur PAUP* v4.0b10-sagteware te gebruik (Swofford 2002). Steekproef-hersteekproef met vervangingswaardes is uitgedruk as persentasies van 1 000 herhalings.
3. Resultate en bespreking
3.1 Selektering van stamme vir verdere identifikasie
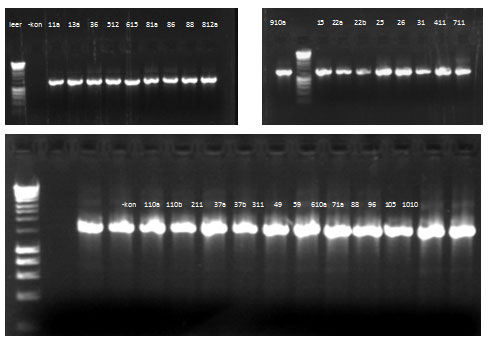
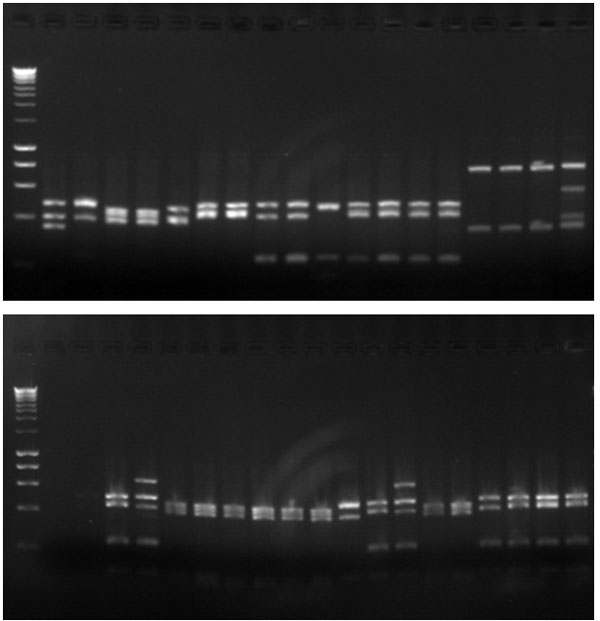
Eenhonderd-en-veertig reinkulture is vanuit die SVK van die perlemoen geïsoleer. Gebaseer op die resultate wat deur Gramkleuring, katalase- en oksidasetoetse verkry is, is 29 kulture vir verdere DNS-ekstraksies gekies (Tabel 1; Figuur 4). Na die suksesvolle isolering en PKR-amplifisering van die genoom-DNS, is die DNS met die beperkingsensiem RsaI gesny om verskillende snydingsprofiele te verkry (Figuur 5a). Gebaseer op die beperkingsfragment-lengteprofiele (Figuur 5b) is 10 verskillende stamme as verteenwoordigers vir die bepaling van die DNS-volgorde gekies.
|
Tabel 1: Opsomming van die eienskappe van geïdentifiseerde bakteriële isolate |
||||||
|
Identifikasie |
Genbank-nr. |
Isolaat-nr. |
Gram-kleuring |
Selmorfologie |
Katalase-toets |
Oksidase-toets |
|
Vibrio nigripulchritudo |
KJ861996 |
110b |
Gram negatief |
Staafvormig |
+ |
+ |
|
Vibrio nigripulchritudo |
KJ861997 |
610a |
Gram negatief |
Staafvormig |
+ |
+ |
|
Photobacterium leiognathi |
KJ861998 |
512a |
Gram negatief |
Staafvormig |
+ |
+ |
|
Paracoccus marcusii |
KJ861999 |
615 |
Gram negatief |
Kokkusvormig |
+ |
+ |
|
Vibrio cyclitrophicus |
KJ862000 |
81a |
Gram negatief |
Staafvormig |
+ |
+ |
|
Vibrio aestuarianus |
KJ862001 |
812a |
Gram negatief |
Staafvormig |
+ |
+ |
|
Staphylococcus carnosus |
KJ862002 |
11a |
Gram positief |
Kokkusvormig |
+ |
- |
|
Staphylococcus equorum |
KJ862003 |
910a |
Gram positief |
Kokkusvormig |
+ |
- |
|
Staphylococcus cohnii |
KJ862004 |
13a |
Gram positief |
Kokkusvormig |
+ |
- |
|
Corynebacterium variabile |
KJ862005 |
22a |
Gram positief |
Staafvormig |
+ |
- |
3.2 Identifisering van geïsoleerde bakterieë
Filogenetiese ontledings van die DNS-volgordes het getoon dat bakterieë wat geklassifiseer is, tot vyf verskillende genera beperk was, insluitende Vibrio, Photobacterium, Corynebacterium, Staphylococcus en Paracoccus. Vyf aparte filogenetiese ontledings is gedoen om hierdie stamme korrek te identifiseer, aangesien hierdie stamme geneties ver verwyderd van mekaar is.
Grampositiewe isolate wat geïdentifiseer is, vorm deel van die genera Corynebacterium en Staphylococcus. Beide hierdie isolate toets positief vir katalase en negatief vir oksidase.
Figuur 4. 1,5% agarose-gel-foto van 16S rRNA PKR-produkte van bakteriële isolate wat geselekteer is op grond van Gramkleuring, katalase- en oksidasetoetse. ’n HyperLadder I (Bioline) leer is gebruik en die gemiddelde grootte van die bande wat verkry is, is 1 200bp
Figuur 5. a. Agarose gel foto van die geamplifiseerde 16S ribosomale DNA wat gesny is met RasI. b. Restriksie-fragment-lengte-profiele wat saamgestel is vanaf agarose gel foto in figuur 3 a. Verskillende bandpatrone dui op moontlike verskillende spesies. ’n HyperLadder I (Bioline) leer is gebruik om die relatiewe groottes van die bande te bepaal.
Corynebacterium variabile is niemotiele, staafvormige selle wat enkel, in pare of in groepe kan voorkom (Collins 1987). ’n Verskeidenheid van Corynebacterium-spesies is al vanaf kaasoppervlakke en ander suiwelprodukte, asook uit grondomgewings en plantmateriaal geïsoleer (Gelsomino e.a. 2005). Alhoewel hierdie spesies nie patogenies is nie, is die groep nie bekend vir enige probiotiese effekte nie en word dit dus nie as ’n potensiële akwakultuurprobiotikum oorweeg nie.
Drie verskillende Staphylococcus-spesies is as S. carnosus, S. equorumen S. cohnii geïsoleer en geïdentifiseer. Daar is nie baie navorsing oor Staphylococcus in akwakultuuromgewings gedoen nie, maar hierdie genus is wel berug vir die bederf van voedsel. Indien enterotoksienbesmette voedsel deur mense ingeneem word, veroorsaak dit gastro-enteritis. Daar is ook bevind dat S. equorum in staat is om lugweginfeksies in persone met fibrose te veroorsaak (Kajikazawa e.a. 2007). As gevolg van die patogenisiteit van hierdie genus word hierdie groep nie as potensiële probiotiese bakterieë oorweeg nie.
Vibrio word algemeen in akwatiese en mariene omgewings gevind. Drie verskillende Vibrio-spesies is geïsoleer, naamlik V. aestuarianus, V. nigripulchritudo en V. cyclitrophicus. Hierdie klein staafvormige selle is Gram-negatief en katalase- en oksidase-positief. Die meeste spesies in hierdie genus het ’n polêre flagellum en is daarom motiel (Tison en Seidler, 1983). Vibrio-spesies word gesien as opportunistiese patogene (Labreuche e.a.2006) en siektes wat deur hierdie genus versprei word, staan bekend as vibriosis en het al groot ekonomiese verliese in akwakultuur tot gevolg gehad het (Goarant e.a. 2007). Twee van die Vibrio-spesies wat in hierdie studie geïsoleer is, naamlik V. aestuarianus, V. nigripulchritudo,is bekend daarvoor dat hulle siektes in die oester- en garnaalbedryf veroorsaak (Garnier e.a. 2008; Goarant e.a. 2007; Labreuche e.a. 2006; Labreuche e.a. 2010; Tison en Seidler 1983). Dit is onbekend of hierdie spesies siektes in perlemoen veroorsaak. Geen oordrag tussen Vibrio-spesies is bekend nie. Virulente gene kan dus maklik tussen spesies oorgedra word (Lorenz en Wackernagel 1994) en daarom word hierdie Vibrio-isolate nie oorweeg om as potensiële probiotiese bakterium gebruik te word nie.
Naverwant aan Vibrio-spesies is die bioluminessente Photobacterium leiognathi,wat ook vanuit die SVK van die perlemoen geïsoleer is. Hierdie Gram-negatiewe staafvormige bakterieë is katalase- en oksidase-positief. Bioluminessente bakterieë in akwatiese omgewings is bekend vir hul simbiotiese verwantskappe met sekere visspesies. Hierdie bakterieë koloniseer die ligorgane van spesifieke visspesies en help so om prooi te lok deur lig uit te straal (Ast e.a. 2007). Hierdie groep bakterieë kan ook help met die voorsiening van suurstof en voedingstowwe vir die gasheer. Oortollige bioluminessente bakteriële selle in hierdie ligorgane word deur die spysverteringskanaal tot die omgewing uitgewerp (Dunlap e.a.2004). Sommige Photobacterium-spesies, soos Photobacterium leiognathi wat in hierdie studie geïsoleer is, kan ook vrylewend wees en is dus nie van die gasheer afhanklik nie (Zarubin e.a. 2012). Alhoewel hierdie bakterieë in die omgewing kan oorleef, is daar dikwels nie genoeg nutriënte vir optimale groei van die selle nie. Hierdie selle bioluminesseer dan om sodoende predatore soos soöplankton te lok. Nadat die selle deur die soöplankton geëet is, begin die bakterieë om lig uit te straal en lok sodoende groter predatore. Deur hierdie proses is die vrylewende bioluminessente selle in staat om die spysverteringskanaal van visse te bereik, waar meer voedingstowwe teenwoordig is as in die omgewing. Die selle kan vinniger in hierdie nutriëntryke omgewing vermeerder en word dan weer saam met die ontlasting na die omgewing uitgeskei (Zarubin e.a. 2012). As gevolg van die vrylewende aard van P. leiognathi word hierdie isolaat nie as ’n potensiële probiotiese bakterium oorweeg nie. Vir ’n bakterium om ’n suksesvolle probiotikum te wees, is kolonisering van die SVK baie belangrik.
Laastens is isolaat 615 as ’n Paracoccus-spesie geïdentifiseer. Gebaseer op die filogenetiese verwantskappe is hierdie isolaat baie naverwant aan drie astasantienproduserende bakterieë, naamlik Paracoccus marcusii, P. carotinifaciens en P. haeundaensis. As gevolg van die naverwante 16S rDNA-gene van hierdie drie spesies kon daar nie deur die filogenetiese ontledings duidelik onderskei word watter een van hierdie spesies die naaste aan die isolaat verwant is nie, alhoewel dit die naaste verwant is aan P. marcusii. Daar word voorgestel dat verdere identifikasie gedoen moet word om te verseker dat die isolaat wel geïdentifiseer kan word as P. marcusii. Al drie hierdie astasantienproduserende spesies vorm oranje kolonies, is Gram-negatief, niesporulerend en katalase- en oksidase-positief. As gevolg van die produksie van astasantien hou al drie hierdie Paraoccus-spesies belowende gebruike vir die akwakultuurbedryf in (Bjerkeng e.a. 1999; Choubert e.a. 2009; Gomes e.a. 2002).
Astasantien word as sekondêre metaboliet deur hierdie drie Paracoccus-spesies geproduseer. Die rooi tot oranje karotenoïdpigment is 'n hoogs aktiewe antioksidant en as gevolg hiervan hou dit belowende voordele vir die gasheer in (Gabaudan, 1996). Hierdie antioksidant-aktiwiteit kan sekere belangrike biologiese funksies in die gasheer bevorder, soos ’n verhoogde beskerming teen oksidatiewe stres en ’n verhoogde seksuele volwassenheid (Gabaudan 1996; Higuera-Ciapara e.a. 2006). Die produksie van die pigment deur hierdie bakterieë hou ook die potensiaal in om as ’n pigmentbron gebruik te kan word. Astasantien word algemeen gebruik as ’n pigment in die voer van sekere akwakultuurspesies, soos forel, salm en garnale (Bjerkeng e.a. 1999; Choubert e.a. 2009; Gomes e.a. 2002). Hierdie waterlewende diere is nie in staat om die pigment te produseer nie, en onder akwakultuurtoestande kom die diere nie in aanraking met die natuurlike pigmente nie. Dit het tot gevolg dat die vleis vaalgrys bly en dus nie vir die verbruiker aanvaarbaar is nie (Higuera-Ciapara e.a. 2006). Astasantien wat by die voer gevoeg word, kan chemies of biologies gesintetiseer word. Beide hierdie bestaande prosesse het verskeie voor-en nadele, maar een van die grootste nadele is dat al twee prosesse redelik duur is (Ausich 1997; Bjerkeng e.a. 2007; Bowen e.a. 2002; Katsuyama e.a. 1987). Astasantien wat deur Paracoccus-spesies geproduseer word, kan moontlik as ’n goedkoper alternatief gebruik word as ’n pigmentbron vir sekere akwakultuurspesies. Verdere studies is nodig om te bepaal of hierdie isolaat die potensiaal inhou om as probiotikum en pigmentbron in akwakultuur gebruik te kan word.
4. Gevolgtrekking
Met die doel om bakterieë in die SVK van perlemoen te isoleer en identifiseer, is daar nege verskillende spesies in hierdie studie geïdentifiseer. Een van hierdie spesies, Paracoccus marcusii, toon potensiaal om as ’n probiotikum ontwikkel te kan word as gevolg van astasantienproduksie. Hierdie isolaat het ook die verdere potensiaal om as ’n koste-effektiewe pigmentbron in akwakultuur gebruik te word. Verdere in vitro- en in vivo-studies word benodig om te bepaal of P. marcusii wel as ’n probiotikum en pigmentbron in akwakultuur gebruik kan word.
Bibliografie
Ast, J.C., H. Urbanczyk en P.V. Dunlap. 2007. Natural Merodiploidy of the lux-rib Operon of Photobacterium leiognathi from Coastal Waters of Honshu, Japan. Journal of Bacteriology, 189(17):48–58.
Ausich R.L. 1997. Commercial opportunities for carotenoid production by biotechnology. Pure and Applied Chemistry,69(10):2169–73.
Austin, B. en A.C. Billaud. 1990. Inhibition of the fish pathogen, Serratia liquefaciens, by an antibiotic-producing isolate of Planococcus recovered from sea water. Journal of Fish Diseases, 13:553–6.
Austin, B., L.F. Stuckey, P.A.W. Robertson, I. Effendi en D.R.W. Griffith. 1995. A probiotic strain of Vibrio alginolyticus effective in reducing diseases caused by Aeromonas salmonicida, Vibrio anguillarum and Vibrio ordalii. Journal of Fish Diseases, 18:93–6.
Balcázar, J.L., I. De Blas, I. Ruiz-Zarzuela, D. Vendrell, A.C. Calvo, I. Marquez, O. Girones en J.L. Muzuiz. 2007. Changes in intestinal microbiota and humoral immune response following probiotic administration in brown trout (Salmo trutta). British Journal of Nutrition, 97:522–7.
Baya, A.M., R.S. Boethling en A. Ramos-Cormenzana. 1981. Vitamin production in relation to phosphate solubilization by soil bacteria. Soil Biology and Biochemistry, 13:527–31.
Bjerkeng, B., B. Hatlen en E. Wathne. 1999. Deposition of astaxanthin in fillets of Atlantic salmon (Salmo salar) fed diets with herring, capelin, sandeel, or Peruvian high PUFA oils. Aquaculture, 180:307–19.
Bjerkeng, B., M. Peisker, K. van Schwartzenberg, T. Ytrestoyl en T. Asgard. 2007. Digestibility and muscle retention of astaxanthin in Atlantic salmon, Salmo salar, fed diets with the red yeast Phaffia rhodozyma in comparison with synthetic formulated astaxanthin. Aquaculture,269:476–89.
Bostock, J., B. McAndrew, B. Richards, K. Jauncey, T. Telfer, K. Lorenzen, D. Little, L. Ross, N. Handisyde, I. Gatward en R. Corner. 2010. Aquaculture: global status and trends. Philosophical Transactions of the Royal Society B, 365:2897–912.
Boudinot, P., M. Blanco, P. de Kinkelin en A. Benmansour. 1998. Combined DNA immunization with the Glycoprotein gene of viral hemorrhagic septicemia virus and infectious hematopoietic necrosis virus induces double-specific protective immunity and nonspecific response in rainbow trout. Virology, 249:297–306.
Bowen, J., C. Soutar, R.D. Serwata, S. Lagocki, D.A. White, S.J. Davies en A.J. Young. 2002. Utilization of (3S,3’S)-astaxanthin acyl esters in pigmentation of rainbow trout (Oncorhynchus mykiss). Aquaculture Nutrition,8:59–68.
Brunt, J. en B. Austin. 2005. Use of a probiotic to control lactococcosis and streptococcosis in rainbow trout, Oncorhynchus mykiss. Journal of Fish Diseases, 28:693–701.
Burr, G. en D. Gatlin. 2005. Microbial ecology of the gastrointestinal tract of fish and the potential application of probiotics and probiotics in finfish aquaculture. Journal of the World Aquaculture Society, 36(4):425–36.
Cabello, F.C. 2006. Heavy use of prophylactic antibiotics in aquaculture: a growing problem for human and animal health and for the environment. Environmental Microbiology, 8(7):37–44.
Choubert, G., J.P. Cravedi en M. Laurentie. 2009. Effect of alternate distribution of astaxanthin on rainbow trout (Oncorhynchus mykiss) muscle pigmentation. Aquaculture, 286:100–104.
Cleveland, J., T.J. Montville, I.F. Nes en M.L. Chikindas. 2001. Bacteriocins: safe, natural antimicrobials for food preservation. International Journal of Food Microbiology, 71:1–20.
Collins, M.D. 1987. Transfer of Arthrobacter variabilis (Muller) to the Genus Corynebacterium, as Corynebacterium variabilis comb. nov. International Journal of Systematic Bacteriology, 37(3):287–8.
Croft, M.T., , A.D. Lawrence, E. Raux-Deery, M.J. Warren en A.G. Smith. 2005. Algae acquire vitamin B12 through a symbiotic relationship with bacteria. Nature, 438:90–3.
Direkbusarakom, S., M. Yoshimizu, Y. Ezura, L. Ruangpan en Y. Danayadol. 1998. Vibrio spp., the dominant flora in shrimp hatchery against some fish pathogenic viruses. Journal of Marine Biotechnology, 6:266–7.
Dunlap, P.V., A. Jiemjit, F.C. Ast, M.M. Pearce, R.R. Marques en C.R. Lavilla-Pitogo. 2004. Genomic polymorphism in symbiotic populations of Photobacterium leiognathi. Environmental Microbiology, 6(2):145–58.
Erasmus, J.H., P.A. Cook en V.E. Coyne. 1997. The role of bacteria in the digestion of seaweed by the abalone Haliotis midae. Aquaculture,155:377–86.
Farzanfar, A. 2006. The use of probiotics in shrimp aquaculture. FEMS Immunology and Medical Microbiology, 48:149–58.
Gabaudan J. 1996. Dietary astaxanthin improves production yield in shrimp farming. Fish Chimes, 16:37–39.
Garcia, S.M. en A.A. Rosenberg. 2010. Food security and marine capture fisheries: characteristics, trends, drivers and future perspectives. Philosophical Transactions of the Royal Society B:365:69–80.
Garnier, M., Y. Labreuche en J.L. Nicolas. 2008. Molecular and phenotypic characterization of Vibrio aestuarianus subsp. francensis subsp. nov., a pathogen of the oyster Crassostrea gigas. Systematic and Applied Microbiology, 31(5):358–65.
Gelsomino, R., M. Vancanneyt, C. Snauwaert, K. Vademeulebroecke, B. Hoste, T.M. Cogan en J. Swings. 2005. International Journal of Systematic and Evolutionary Microbiology, 55:29–31.
Goarant C., Y. Reynaud, D. Ansquer, S. de Decker en F. Merien. 2007. Sequence polymorphism-based identification and quantification of Vibrio nigripulchritudo at the species and subspecies level targeting an emerging pathogen for cultured shrimp in New Caledonia. Journal of Microbiological Methods, 1–15.
Gomes, E., J. Dias, P. Silva, L. Valente, J. Empis, L. Gouveia, J. Bowen en A. Young. 2002. Utilization of natural and synthetic sources of carotenoids in the skin pigmentation of gilthead seabream (Sparus aurata). European Food Research and Technology, 214:287–93.
Grinde, B., O. Lie, T. Poppe en R. Salte. 1988. Species and individual variation in lysozyme activity in fish of interest in aquaculture. Aquaculture, 69:299–304.
Guglielmetti, E., J.M. Korhonen, J. Heikkinen, L. Morelli en A. von Wright. 2009. Transfer of plasmid-mediated resistance to tetracycline in pathogenic bacteria from fish and aquaculture environments. Federation of European Microbiological Societies, 293:28–34.
Harris, J.M. 1993. The presence, nature and role of gut microflora in aquatic invertebrates: a synthesis. Microbial Ecology, 25:195–231.
Harzevili, A.R.S., H. van Duffel, P. Dhert, J. Swings en P. Sorgeloos. 1998. Use of a potential probiotic Lactococcus lacis AR21 strain for the enhancement of growth in the rotifer Brachionus plicatilis (Müller). Aquaculture Research, 29:411–17.
Heuer, O.E., H. Kruse, K. Grave, P. Collignon, I. Karunasagar en F.J. Angulo. 2009. Human health consequences of use of antimicrobial agents in aquaculture. Clinical Infectious Diseases, 49:48–53.
Higuera–Ciapara, I., Felix–Valenzuela, L. en Goycoolea, F.M. 2006. Astaxanthin: A review of its chemistry and applications. Critical Reviews in Food Science and Nutrition, 46:185–196.
Hirsch, R., T. Ternes, K. Haberer en K.L. Kratz. 1999. Occurrence of antibiotics in the aquatic environment. The Science of the Total Environment, 225:109–18.
Kajikazawa, T., T. Sugita en A. Nishikawa, A.2007.Comprehensive identification of bacteria in processed fresh edible sea urchin using 16S ribosomal DNA sequence analysis: The products contain various food poisoning-related bacteria and opportunistic bacterial pathogens. Journal of Health Science, 53(6):756–9.
Kamei, Y., M. Yoshimizu, Y. Ezura en T. Kimura. 1988. Screening of bacteria with antiviral activity from fresh water salmonid hatcheries. Microbiology immunology,32(1):67–73.
Katsuyama, M., T. Komori en T. Matsuno. 1987. Metabolism of three stereoisomers of astaxanthin in the fish, rainbow trout and tilapia. Comparative Biochemistry and Physiology,86(1):1–5.
Kim, D.H. en B. Austin. 2006. Innate immune responses in rainbow trout (Oncorhynchus mykiss, Walbaum) induced by probiotics. Fish and Shellfish Immunology, 21:513–24.
Kümmerer, K. 2009. Antibiotic in the aquatic environment – A review. Chemosphere, 75:417–34.
Labreuche, Y., C. Lambert, P. Soudant, V. Boulo, A. Huvet en J.L. Nicolas. 2006. Cellular and molecular hemocyte responses of the Pacific oyster, Crassostrea gigas, following bacterial infection with Vibrio aestuarianus strain 01/32. Microbes and Infection, 8(12):15–24.
Labreuche, Y., F. le Roux, J. Henry, C. Zatylny, A. Huvet, C. Lambert, P. Soudant, D. Mazel en J.L. Nicolas. 2010. Vibrio aestuarianus zinc metalloprotease causes lethality in the Pacific oyster Crassostrea gigas and impairs the host cellular immune defences. Fich and Shellfish Immunology, 29:753–8.
Lorenz, M.G. en W. Wackernagel. 1994. Bacterial gene transfer by natural genetic transformation in the environment. Microbiological Reviews, 58(3):563–602.
Macey, B.M. en V.E. Coyne. 2005. Improved growth rate and disease resistance in farmed Haliotis midae through probiotic treatment. Aquaculture,245:249–61.
—. 2006. Colonization of the gastrointestinal tract of the farmed South African abalone Haliotis midae by the probionts Vibrio midae SY9, Cryptococcus sp. SS1 and Debaryomyces hansenii AY1. Marine Biotechnology,8:246–59.
Martin, J.F., E. Gudina en J. Barredo. 2008. Conversion of β–carotene into astaxanthin: Two separate enzymes or a bifunctional hydroxylase–ketolase protein? Microbial Cell Factories,7(3):1–10.
Merchie, G., P. Lavens en P. Sorgeloos. 1997. Optimization of dietary vitamin C in fish and crustacean larvae: a review. Aquaculture, 155:165–81.
Muraosa, Y., K. Morimoto, A. Sano, K. Nishimura en K. Hatai. 2009. A new peronosporoycete, Halioticida noduliformans gen. Et sp. nov., isolated from white nodules in the abalone Haliotic spp. from Japan. Mycoscience, 50:106–15.
Nayak, S.K. 2010. Probiotics and immunity: A fish perspective. Fish and Shellfish Immunology, 29:2–14.
Naylor, R.L., R.J. Goldburg, J.H. Primavera, N. Kautsky, M.C.M. Beveridge, J. Clay, C. Folke, J. Lubchenco, H. Mooney en M. Troell. 2000. Effect of aquaculture on world fish supplies. Nature, 405:17–24.
Panigrahi, A., V. Kiron, T. Kobayashi, J. Puangkaew, S. Satoh en H. Sugita. 2004. Immune responses in rainbow trout Oncorhynchus mykiss induced by a potential probiotic bacteria Lactobacillus rhamnosus JCM 1136. Veterinary immunology and immunopathology, 102:379–88.
Poston, H.A. 1964. Effect of dietary vitamin K and sufaguanidine on blood coagulation time, microhematocrit and growth of immature brook trout. Progressive Fish Culturist, 26:59–64.
Rengpipat, S., W. Phianphak, S. Piyatiratitivorakul en P. Menasveta. 1998. Effects of a probiotic bacterium on black tiger shrimp Penaeus monodon survival and growth. Aquaculture, 167:301–13.
Rigos, G. en G.M. Troisi. 2005. Antibacterial agents in Mediterranean finfish farming: A synopsis of drug pharmacokinetics in important euryhaline fish species and possible environmental implications. Reviews in Fish Biology and Fisheries, 15:53–73.
Rimstad, E. 2011. Examples of emerging virus diseases in salmonid aquaculture. Aquaculture Research, 42:86–9.
Ringø, E. 1999. Lactic acid bacteria in fish: antibacterial effect against fish pathogens. In COST 98. Effects of Antinutrients on the Nutritional Value of Legume Diets. Antinutrients – for better or for worse? Interactions with Intestinal Physiology and Microbiology. European Commission, 1999.
Sargent, J.R. 1997. Fish oils and human diet. British Journal of Nutrition, 78:5–13.
Sugita, H., C. Miyajima en Y. Deguchi. 1991. The vitamin B12-producing ability of the intestinal microflora of freshwater fish. Aquaculture, 92:267–76.
Swofford, D.L. 2002. PAUP*: phylogenetic analysis using parsimony (*and other methods). Version 4.0b10. Sunderland, MA: Sinauer Associates.
Tapiero, H., D.M. Townsend en K.D. Tew. 2004. The role of carotenoids in the prevention of human pathologies. Biomedicine and Pharmacotherapy,58:100–10.
Ten Doeschate, K.I. en V.E. Coyne. 2008. Improved growth rate in farmed Haliotis midae through probiotic treatment. Aquaculture,284:174–9.
Thompson, J.D., T.J. Gibson, F. Plewniak, F. Jeanmougin en D.G. Higgins. 1997. The ClustalX windows interface: flexible strategies for multiple sequence alignment aided by quality analysis tools. Nucleic Acids Research, 24:4876–4882.
Tidwell, J.H. en Allan, G.L. 2001. Fish as food: aquaculture’s contribution. European Molecular Biology Organization Reports, 2(11):958–63.
Tison, D.L. en R.J. Seidler. 1983. Vibrio aestuarianus: a new species from estuarine waters and shellfish. International Journal of Systematic Bacteriology, 33(4):699–702.
Venkat, H.K., N.R. Sahu en K.K. Jain. 2004. Effect of feeding Lactobacillus-based probiotics on the gut microflora, growth and survival of postlarvae of Macrobrachium rosenbergii. Aquaculture Research, 35:501–7.
Verschuere, L., G. Rombaut, P. Sorgeloos en W. Verstraete. 2000. Probiotic bacteria as biological control agents in aquaculture. Microbiology and Molecular Biology Reviews,64(4):655–71.
Vine, N.G., W.D. Leukes en H. Kaiser. 2006. Probiotics in marine larviculture. Federation of European Microbiological Societies, 30:404–27.
Vine, N.G., W.D. Leukes, H. Kaiser, S. Daya, J. Baxter en T. Hecht. 2004. Competition for attachment of aquaculture candidate probiotic and pathogenic bacteria on fish intestinal mucus. Journal of Fish Diseases, 27:319–26.
Wang, Y.B. 2007. Effect of probiotics on growth performance and digestive enzyme activity of the shrimp Penaeus vannamei. Aquaculture, 269(4):259–64.
Wang, Y.B., J.R. Li en J. Lin. 2008. Probiotics in aquaculture: Challenges and outlook. Aquaculture, 281:1–4.
Zarubin, M., S. Belkin, M. Lonescu A. en Genin. 2012. Bacterial bioluminescence as a lure for marine zooplankton and fish. Proceedings of the National Academy of Science USA,109(3):853–7.
Erkenning
Ons bedank graag vir Abagold-perlemoenplaas (Hermanus, Suid-Afrika) vir die voorsiening van die perlemoen.
LitNet Akademies (ISSN 1995-5928) is geakkrediteer by die SA Departement Onderwys en vorm deel van die Suid-Afrikaanse lys goedgekeurde vaktydskrifte (South African list of Approved Journals). Hierdie artikel is portuurbeoordeel vir LitNet Akademies en kwalifiseer vir subsidie deur die SA Departement Onderwys.