|
||||||||||
Epigenetika verwys na oorerflike en verbygaande variasie in geenuitdrukking en proteïenvouing wat nie bepaal word deur variasie in DNA-basisvolgorde of proteïen-aminosuurvolgorde nie. Epigenetiese variasie word moontlik gemaak deur DNA-metilering, histoonmodifikasie, regulering deur verskeie vorme van niekoderende RNA en prion-bemiddelde variasie in proteïenvouing. DNA-metilering, histoonmodifikasies en niekoderende RNA is nukleïensuurverwante epigenetiese meganismes wat geenuitdrukking beïnvloed. Prions, daarenteen, verteenwoordig ’n proteïenverwante epigenetiese meganisme wat proteïenvouing en gevolglik proteïenfunksie beïnvloed. Die genoom, epigenoom en omgewing saam bepaal die fenotipe. Moduleerders van die epigenoom het die grootste impak tydens oorgangsfases in ontwikkeling, byvoorbeeld rondom bevrugting en vroeë fases van die embrio, , anders as hul impak op die epigenoom van gedifferensieerde selle. Epigenetiese “littekens” wat vroeg in die lewe deur omgewingsfaktore geïnduseer word, hou implikasies in vir gesondheid in volwassenheid. Kennis oor die verhouding tussen die epigenoom, omgewing en siekte is steeds vaag. Dit is onduidelik of die omgewing ’n direkte of indirekte impak op die epigenoom het en of klein veranderinge in die epigenoom die oorsaak of gevolg van siekte is. Epigenetiese variasie geassosieer met siektes kan gebruik word as biomerkers vir siektevatbaarheid indien dit teenwoordig is in die voorafbestaande epigenoom. Epigenetiese variasie deur siekte geïnduseer kan gebruik word om die erns en duur van siekte of die uitkoms van behandeling te monitor. ’n Verskeidenheid molekulêr-biologiese en biochemiese tegnieke word gebruik om epigenetiese variasie te bestudeer. Die keuse van tegniek is afhanklik van die tipe epigenetiese meganisme wat bestudeer word, die doel van die studie, en, in die geval van nukleïensuurverwante meganismes, of die modifikasie op genoom-wye, streek- of lokus-spesifieke vlak bestudeer word. In hierdie oorsigsartikel word epigenetika bespreek onder die temas: agtergrond, tipes, oorerflikheid, moduleerders, gesondheid en siekte, en metodes ter bestudering.
Epigenetika regverdig die herskryf van die moderne evolusieteorie. Dit ondersteun die oorerwing van verworwe eienskappe en werp nuwe lig op meganismes wat inligting kommunikeer vanaf die omgewing na die genoom, transkriptoom en proteoom.
Trefwoorde: epigenetika; genetika; omgewing; evolusie
Epigenetics: The link between genetics and environment
All living organisms face the constant challenge of adapting to an ever changing environment. The mechanisms that bring about adaptation have been under investigation for centuries. Aristotle (384 BC–322 BC), the Greek philosopher and author of the theory of epigenesis, postulated that each embryo of an organism develops systematically from an undifferentiated mass. Epigenesis was the first theory to point to development based on specific cues. It contrasted with preformation: the idea that all organisms develop from miniature versions of themselves in the gametes. Jean-Baptiste Lamarck (1744–1829), a French naturalist and author of the term biology, published the first formal theory of evolution in which he proposes two laws of evolution – the law of use or disuse and the law of inheritance of acquired characteristics. In his theory of natural selection Charles Darwin (1809–1882) postulated that subtle variation in the phenotype of an organism, favouring survival, will be carried over to the offspring. In The Origin of Species (1859) Darwin describes two forces in evolution – natural selection and conditions of existence (environment). Of these two forces, Darwin argues the latter to be more powerful, implying that natural selection can take place only within the boundaries of a specific environment.
The term epigenetics was coined by Conrad Waddington in 1942, and he defined it as the interaction between genes and the environment to produce phenotype. Today epigenetics is widely used to refer to the heritable and transient changes in gene expression not caused by nucleotide sequence variation, but collectively instigated by epigenetic marks classified as DNA methylation, histone modification and non-coding RNA. In addition to these nucleic-acid-related modifications, prion-mediated variation in protein folding was more recently identified as a protein-conformation-based epigenetic mechanism in baker’s yeast. Epigenetic marks respond to changes in the environment, allowing adaptation. Unlike the genome, plasticity of the epigenome is observed over a short time, responding to, and dictating change within, one generation. The phenotype is therefore determined by the interaction between the genome, epigenome and environment.
The most widely studied and best understood epigenetic modification is DNA methylation. The methylation of a DNA sequence involves the covalent binding of a methyl group on the 5th carbon position of a cytosine ring in a reaction catalysed by DNA methyl transferase 1 (DNMT-1). Cytosine methylation occurs largely in the context of CpG dinucleotides and clusters of these dinucleotides are known as CpG islands (CGIs). The epigenome undergoes major reprogramming marked by global demethylation during early embryogenesis when paternal and maternal genomes merge to form the zygote and during gametogenesis in the primordial germ cells (PGCs) of the embryo. Lineage-specific DNA methylation patterns are established by de novo DNA methyl transferases, DNMT3A and DNMT3B, around implantation and are maintained by DNMT-1. Intrinsic and extrinsic (environmental) factors influence the establishment and maintenance of epigenetic marks.
DNA and histone methylation hinge on the level of S-adenosylmethionine (SAM), the universal methyl donor generated by the methionine (one-carbon) cycle in interaction with the folate cycle. During specific stages of development the epigenome is selectively demethylated, bestowing a unique epigenetic signature on each cell type. DNMT-1 maintains methylation patterns and abnormal hypomethylation is a cause of altered gene expression in diseased tissue. In addition to DNA methylation, specific modifications on histones form a second epigenetic mechanism vital in gene regulation. Histones are small, highly basic nuclear proteins that function to stabilise and package chromatin. Specific modifications in an unstructured domain at the N-terminal of most histones allow epigenetic control of gene expression through changes in accessibility of the DNA sequence to transcription factors and other regulatory proteins. Histone modification is characterised by complex and diverse chemical changes, including acetylation, methylation, phosphorylation and ubiquitination.
Unlike DNA methylation and histone modifications that silence genes by preventing transcription, non-coding RNA (ncRNA) prevents translation of mRNA to proteins (silencing). ncRNA, among which small nucleolar RNA (snoRNA), micro-RNA (miRNA), small interfering RNA (siRNA), piwi-interacting RNA (piRNA), and long non-coding RNA (lnRNA), form part of the RNA-induced silencing complex (RISC). RISC regulates gene expression through complementary (specific and less specific) base pairing between the ncRNA and target mRNA/DNA leading to the cleavage of the nucleotide target sequence by means of a DICER enzyme.
A form of extreme epigenetics is seen in prions. Prions are a group of proteins with the unique capacity to fold into different conformations. They are stable conformational variants of normal proteins with distinct functions. Extreme environmental stress induces proteins to take on the prion conformation, a process that is reversible when the stress is relieved. Prion conformations are stably carried over to daughter cells during mitosis and meiosis, thereby allowing the inheritance of stress-induced acquired characteristics. In humans prions have mostly been associated with disease , but recent reports on baker’s yeast show that prion induction favours survival of the organism in altered environments. The altered patterns of protein folding in the organism, induced by the environment and inherited by offspring, can therefore be considered as an epigenetic mechanism allowing adaptation. Future work on prions in mammals may reveal their role in the maintenance of physiological conditions in ever changing environments.
The epigenome is particularly sensitive to modification at conception, during gestation, around birth and during puberty. Epigenetic “scars” induced early in life may hold implications for health in adulthood. Transgenerational inheritance of alterations in the epigenome induced by environment remains controversial. Only marks transmitted to the F3 generation are truly transgenerational since in utero exposure effectively exposes the mother (F0), the foetus (F1) and primordial germ cells of the foetus (F2). Much remains to be learned about the epigenome; the hierarchical order, interdependency and interplay of epigenetic mechanism, as well as the processes dictating the loci in the genome where methylation is established and maintained. Environmental factors such as a diet rich in methyl donors has been shown to alter the coat colour of Agouti mice. Paternal alcohol use is linked to the development of foetal alcohol spectrum disorders caused by hypomethylation of two imprinted genes in sperm DNA. Besides diet and lifestyle, the psychological environment during early development and genetic factors can also modulate the epigenome.
Regarding the relation between the epigenome, environment and diseases it is unclear whether environment directly or indirectly impacts the epigenome and whether small changes in the epigenome are the cause or effect of disease. Nonetheless, epigenetic marks associated with disease could serve as biomarkers of disease risk when present in a pre-existing epigenome, while disease-reactive epigenetic changes may serve to monitor disease severity, duration or treatment outcome. Manipulating the epigenome for therapeutic benefit is already illustrated in cancer treatment. Epigenetics holds important implications for study design; genetics, epigenetics and environment need to be considered in disease association studies. The cell-type-specific nature of the epigenome excludes the analysis of mixed cell populations in the study of the epigenome. A wide range of molecular biology techniques are used to study epigenetic variation. The choice of technique depends on the goal of the study and, in the case of nucleic-acid-related epigenetic changes, whether variation will be investigated at a genome-wide, regional, or site-specific level. In this review epigenetics is addressed under the themes: background, types, heritability, modulators, health and diseases, as well as methods for the study of epigenetics. Epigenetics may hold significant implications for diseases known to be influenced by an impoverished environment and common to sub-Saharan Africa, such as tuberculosis, HIV/AIDS and malaria.
Keywords: epigenetics; genetics; environment; evolution
1. Inleiding
Die natuurlike omgewing verander voortdurend en lewende organismes het die uitdaging om hierby aan te pas. Sedert die antieke Griekse tyd word meganismes van aanpasbaarheid en oorerflikheid ontrafel.
1.1 Geskiedenis
Die verlengde hoofde van Macrocephali oortuig Hippokrates (ong. 460 v.C.–370 v.C.) dat verworwe eienskappe oorerflik is (Adams 1891). Die teorie van epigenese, die stelselmatige ontwikkeling van organismes uit ’n ongedifferensieerde massa, word deur Aristoteles (384 v.C.–322 v.C.) voorgestel. William Harvey (1578-1657) se gevolgtrekking dat elke dier uit ’n enkele eiersel ontstaan, lê die grondslag vir moderne embriologie (1651).
Die eerste formele evolusieteorie word deur Jean-Baptiste Lamarck (1744–1829) gepubliseer, waarin hy die wet van gebruik of onbruik en die wet van oorerwing van verworwe eienskappe voorstel (Lamarck 1809). Charles Darwin (1809–1882) se teorie van natuurlike seleksie in The Origin of Species (1859) stipuleer dat subtiele variasie in fenotipe, wat oorlewing en aanwas bevoordeel, oorgeërf word. Hy beskryf twee kragte in evolusie: natuurlike seleksie en die kragtiger “kondisies van bestaan” (omgewing). Hiermee impliseer hy dat natuurlike seleksie binne die grense van omgewing funksioneer. Darwin beskou egter The Origin of Species as ’n onvolledige beskrywing van die teorie van evolusie (Darwin 1888). Later bestudeer hy die bron van variasie waarop natuurlike seleksie inwerk en koppel sommige variasie in organismes aan omgewingsvariasie. In The Variation in Animals and Plants under Domestication (Darwin, 1868) ontwikkel hy die hipotese van pangenese, ’n teorie wat poog om te verklaar hoe omgewingsverworwe fisiologiese veranderinge oorgeërf word, selfs al kodeer genetiese inligting nie daarvoor nie (Darwin 1868). Pangenese word egter deur wetenskaplikes verwerp. Gregor Mendel (1822–1884) se wiskundige model verklaar hoe fenotipe deur genotipe bepaal word en dat genotipe oorgeërf word en herkombineer om nuwe variasies te skep (1866).
August Weismann (1834-1914) formuleer sy teorie van kiemplasma-kontinuïteit in 1883. Die oorspronklike publikasie (1892) word in 1893 in Engels vertaal. Hy erken kiemselle (eier- en spermaselle) as agente van oorerflikheid wat kiemplasma van generasie tot generasie oordra, geïsoleerd van liggaamselle (die Weismann-versperring) en omgewingsimpak. Hy ignoreer omgewingsargumente van Lamarck en Darwin in sy publikasie All-sufficiency of natural selection. Weismann se bisarre “bewys” hiervan is dat muise waarvan die sterte na geboorte afgekap is, oor vele generasies geen kortstert-muise oplewer nie (Weismann 1889). Hans Spemann bevestig dat alle genetiese informasie wat nodig is om ’n nuwe organisme te skep omvat is in vroeë embrioniese selle (1902).
In terme van molekulêre biologie het die werk van Avery, MacLeod en McCarty (1944) aangetoon dat DNA die genetiese materiaal in selle is. Watson en Crick se oplossing van die DNA-struktuur in 1953 is ’n groot molekulêre mylpaal en verklaar die meganisme waardeur gene gekopieer en oorgeërf word.
Conrad Waddington (1905–1975) is die eerste wetenskaplike wat die term epigenetika gebruik (1942), afgelei van Aristoteles se teorie van epigenese. Waddington definieer epigenetika as die interaksie van gene met hul omgewing om fenotipe na vore te bring (Waddington 1942). Volgens Waddington word ontwikkeling bepaal deur die interaksie van gene met mekaar en met die omgewing. Hy kritiseer Neo-Darwinisme en promoveer ’n minder geen-gesentreerde, meer holistiese benadering tot biologie waarbinne die interaksie tussen organisme en omgewing bestudeer kan word.
1.2 Die Mensgenoom-projek
Op 26 Junie 2000 ontmoet Francis Collins, hoof van die Mensgenoom-projek, en Craig Venter, van Celera Corporation, Bill Clinton in die Withuis om die voltooiing van die konsepvolgorde van die mensgenoom te vier. Die genoom is die volledige genetiese komplement van ’n sel of organisme. Die mens het na raming 20 tot 25 duisend gene in sy genoom (Lesk 2008) wat georganiseer is in 25 verskillende DNA-molekules, waarvan 24 as chromosome in die selkern voorkom. Die Mensgenoom-projek was die internasionale projek om alle gene van die mens te karteer en die volgorde van die genoom te bepaal. “It will revolutionize the diagnosis, prevention, and treatment of most, if not all, human diseases,” kondig Clinton aan. Agt maande later is die eerste volgorde van die mensgenoom gepubliseer (International Human Genome Sequencing Consortium 2001). Later erken Collins (2010) dat die president wys was om nie teikendatums aan sy voorspellings te koppel nie. Die bepaling van die genoomvolgorde was ’n merkwaardige mylpaal met groot impak op die mediese wetenskap. Nogtans is daar tot dusver ’n klein fraksie van die oorerflikheid van algemene siektes ontrafel. Genoomvolgorde alleen blyk onvoldoende te wees om al die vrae van die mediese wetenskap te beantwoord.
1.3 Geenaktiwiteit
Gene is nie altyd aktief besig om proteïen of RNA te produseer nie, maar is soms afgeskakel, of hul vlak van aktiwiteit wissel. Tydens die ontwikkeling van ’n organisme vanaf ’n enkele sel flits duisende gene aan en af in komplekse patrone om sel-, weefsel- en orgaandifferensiasie te dikteer. Transkripsiefaktore herken spesifieke DNA-volgordes in geenpromotors en skakel gene aan. DNA-verpakking beïnvloed ook geenuitdrukking. Chromosome is die hoogste orde van DNA-verpakking en bestaan uit chromatienvesels wat uit gevoude nukleosoomkettings bestaan. Nukleosome is die herhalende strukturele eenhede van chromatien, en bestaan uit DNA gedraai om ’n histoon-oktameer, die DNA-bindende proteïen wat die primêre proteïenkomponent van chromatien is. Digverpakte DNA (heterochromatien) se gene is ontoeganklik en onaktief. Minder-digverpakte DNA (euchromatien) bevorder geenuitdrukking. Chromatien is ’n dinamiese struktuur en hermodulering is kritiek vir geenuitdrukking.
1.4 Epigenetika
Sedert die negentigerjare word die term epigenetika algemeen gebruik. Epigenetika is die studie van oorerflike veranderinge in geenuitdrukking wat nie veranderinge in DNA-volgorde betrek nie en deur seldeling oorgedra kan word. Epigenetiese meganismes sluit in:
- DNA-metilering: Die kovalente binding van ’n metielgroep (-CH3) aan meestal sitosien van CG-dinukleotiede. Om verwarring met ’n C-G-basispaar te vermy, word dit aangetoon as CpG: ’n sitosien gevolg deur guanien gekoppel deur middel van ’n fosfodiësterbinding.
- Histoonmodifikasie: Die posttranslasionele modifikasie deur asetilering, fosforilering, metilering en ubikwitinering van histone se N-terminale domeine om so toegang tot die nukleosomale DNA te kontroleer.
- Nie-koderende RNA (ncRNA): RNA wat nie lei tot proteïenproduksie nie, maar wat aan die regulasie van geenuitdrukking deelneem.
- Prions: Stabiele proteïenstrukture met alternatiewe vouing as hul normale eweknieë met identiese aminosuurvolgorde. Hul dien as templaat om normale makkers te oortuig om die alternatiewe vouing en funksie aan te neem.
Die epigenoom is die somtotaal van alle epigenetiese merke van ’n sel op ’n spesifieke stadium van ontwikkeling of onder spesifieke omstandighede. Terwyl die genoom van ’n organisme grootliks staties is binne een generasie en identies is in elke sel, is die epigenoom dinamies en seltipe-spesifiek. Jou basiese epigenoom soos van jou ouers geërf, word voor geboorte binne twee maande na bevrugting neergelê en is onmiddellik onderhewig aan ontwikkeling- of omgewingstimuli. Epigenetiese variasie verleen aan die genoom plastisiteit. Die epigenoom is al beskryf as die “sagteware” wat die “hardeware”, die genoom, dryf. Epigenetiese merke is omkeerbaar en soms oorerflik.
1.5 Nuwe mikpunt
’n Nuwe doelwit in molekulêre genetika is die begrip van genoomfunksie: die integrasie van genetiese inhoud, geenaktiwiteit en proteïenfunksies. Die Encyclopedia of DNA Elements (ENCODE) projek en die US National Institutes of Health (NIH) Roadmap Epigenomics Program, wat afsonderlik in 2003 en 2008 geloods is, identifiseer die posisie van gene in die genoom (proteïenkoderend en niekoderend) en patrone wat bepaal of gene aan- of afgeskakel is in spesifieke weefsel – patrone van chromatienmodifikasie, transkripsiefaktore en DNA-metilering.
1.6 Toepassing van epigenetika
Epigenetika is reeds in die konteks van verskeie navorsingsvelde bestudeer.
Verandering in die epigenetiese prosesse is aangetoon in verskeie soorte kankers in die mens. Ongewone DNA-metilering is die beste epigenetiese waarmerk van kanker (Robertson 2005). Kankerselle word gekenmerk deur beide globale en geenspesifieke verlies aan DNA-metilering sowel as hipermetilering van spesifieke promotors (Jones en Baylin 2007; Portela en Esteller 2010). Sekere teenkankermiddels se werking moduleer epigenetiese meganismes. Manipulasie van die epigenoom vir terapeutiese voordeel is reeds geïllustreer in kankerbehandeling (opgesom in Handel et al. 2010).
Navorsing op diermodelle toon dat voeding en omgewing tydens ontwikkeling lokusspesifieke veranderinge in die epigenoom tot gevolg mag hê. ’n Dieet ryk aan metieldonors metileer ’n lokus stroom-op vanaf die “agouti viable yellow”- (Avy-) alleel en onderdruk die uitdrukking van dié geenvariant wat verantwoordelik is vir geel pelskleur, vetsug en diabetes in muise (Yen et al. 1994). Navorsing op muise en die mens ondersteun ‘n skakel tussen veranderinge in DNA-metilering en verstandelike gestremdheid van kinders met fetale alkoholsindroom, verwek deur ouers met hoë alkoholinname rondom bevrugting (Liu et al. 2009; Ouko et al. 2009).
Sielkundige aspekte van ons vroeë ontwikkeling kan ook die epigenoom beïnvloed. Gereelde moederlike versorging van rotjies na geboorte toon ’n afname in DNA-metilering van die promotor van die geen wat kodeer vir die glukokortikoïed-reseptor in hul breinweefsel. Dit is geassosieer met ’n matiger respons op stres in vergelyking met angstige rotjies wat nie so gekoester is nie (Weaver et al. 2004). Soortgelyke veranderinge in die glukokortikoïed-reseptor was afwesig in die breinweefsel van selfmoordgevalle waar die betrokke persone as kinders mishandel is in vergelyking met selfmoordgevalle sonder ’n geskiedenis van mishandeling (McGowan et al. 2009).
1.7 Belang van epigenetika
Epigenetika het die potensiaal om lig te werp op vrae rakende evolusie en die oorerwing van verworwe eienskappe. Dit kan bydra tot die ontwikkeling van epigenetiese epidemiologie wat die integrasie van genetika, epigenetika, fenotipe en omgewingsinligting benodig. Epigenetika het implikasies vir openbare gesondheid as voorspeller van vatbaarheid, merker van blootstelling, gids in prognose, en teiken vir terapie. Verder beklemtoon epigenetika die belang van omgewingsbewaring, aangesien ’n verwaarlooste omgewing ons epigenoom nadelig kan herprogrammeer. ’n Gesonde epigenoom is krities vir die volhoubaarheid van lewe. Dit gee nuwe betekenis aan ons strewe om moreel om te gaan met onsself, ons naaste en die omgewing. Dit lewer tasbare bewyse van die beloning indien ons dit sou doen.
2. Tipes epigenetiese modifikasies
Nukleïensuurverwante epigenetiese modifikasies word bewerk deur DNA-metilering, histoonmodifikasie en RNA-regulering, wat van mekaar afhanklik is. ’n Verdere epigenetiese variasie, wat nie verband hou met nukleïensuurverwante veranderings nie, is prion-bemiddelde vouing van proteïene.
2.1 DNA-metilering
Metilering van DNA is vir die eerste keer in 1948 waargeneem. Onder natuurlike omstandighede speel hierdie modifikasies ’n betekenisvolle rol in die regulering van geenuitdrukking. Die oorerflike toevoeging van ’n metielgroep tot die vyfde koolstofposisie op ’n sitosienring (5mC) vorm die basis van DNA-metilering (Singal en Ginder 1999). Die reaksie word gekataliseer deur DNA-metieltransferase (DNMT) en vind grootliks plaas op sitosienbasisse gevolg deur guanien (CpG). Met die uitsondering van ingeprente gene ondergaan die epigenoom in primordiale kiemselle en in die sigoot globale demetilering gedurende gametogenese en vroeë embriogenese. ’n Nuwe DNA-metileringspatroon word gevestig deur de novo DNMT3a en 3b.
Figuur 1 gee ’n skematiese voorstelling van die soogdier-metiloom. Streke van die genoom wat ryk is aan sitosien-guanien-dinukleotiede staan bekend as CpG-eilande (CGI) en kom veral voor in die promotors van gene. In eukariote is 70-80% van alle CpG-dinukleotiede gemetileer, met die uitsondering van CGI, wat meestal ongemetileerd is (Goll en Bestor 2005). Die aanvanklike waarneming van CpG-eilande in promotors het tot die aanname gelei dat DNA-metilering geenuitdrukking hoofsaaklik vanuit promotors reguleer, maar die onlangse ontdekking van intrageniese CpG-metilering trek hierdie aanname in twyfel (Ndlovu et al. 2011). Behalwe vir CpG-metilering vind metilering ook plaas op sitosienbasisse in CpHpG- en CpHpH-trinukeiotied-volgordes (H = A, T, of C), maar sulke metileringspatrone verteenwoordig ’n skamele 3% van die totale metiloom (Sigurdsson et al. 2009). Alhoewel hierdie “nie-CpG”-metilering in ’n betreklik lae persentasie voorkom in die volwasse genoom, is tot 20% van die DNA in mens embrioniese stamselle só gemetileer en volgens Ndlovu et al. (2011) wag die uitdaging om die funksie en meganismes van hierdie metileringspatrone te ontrafel op navorsers.

Figuur 1. ’n Skematiese voorstelling van die soogdier-metiloom. Die verspreiding van gemiddelde metilering is gekarteer op ’n geenmodel. Drie gene, A, B en C, word voorgestel in pienk, groen en blou met grys intergeniese areas. CGI’s (CHCHCHCH) kom voor in die promotors van gene, bo-oor die transkripsie-beginpunt (TSS). CGI kom ook voor by intron-ekson-aansluitings, in introne soos weeskinders, of intergeniese areas (grys). CGI-“strande” is areas ryk aan CG-dinukleotiede rondom promotor-CGI’s en kan tot 2 kb vanaf ’n promotor lê. CGI-strande word hoofsaaklik gekenmerk deur differensiële metilering in die meeste weefsel, wat lei tot differensiële geenuitdrukking. “Wees”-CGI’s is eweredig versprei in die geenliggaam, weg van die promotor en tussen eksons. “Wees”-CGI’s word dikwels geassosieer met alternatiewe transkripsie-beginpunte en kan moontlik die promotors van onbekende gene of niekoderende RNA verteenwoordig. (Gebaseer op Ndlovu et al. 2011)
Verskeie studies bevestig dat CGI-metilering in promotors tesame met die afwesigheid van geenliggaam-metilering grootliks gepaard gaan met die demping van geenuitdrukking (Singal en Grinder 1999; Portela en Esteller 2010), terwyl die geenliggaam van aktiewe gene gemetileer is en die promotors ongemetileerd bly. Die spesifieke meganismes van geenonderdrukking deur DNA-metilering by promotors word voorgestel in Figuur 2. DNA-metilering van CGI kan geenuitdrukking direk benadeel deur die binding van transkripsiefaktore (TF’s) aan transkripsiefaktor-bindingsentrums (TFBS’s) te blokkeer (Tate en Bird 1993). Hierdie meganisme is lokus-spesifiek, omdat ’n enkele metielgroep op ’n TFBS die uitdrukking van ’n geen kan belemmer mits die TF metilering-sensitief is. In ’n tweede meganisme word sekere onderdrukkerproteïene deur gemetileerde CGI gewerf, soos die metielsitosien-bindingsdomeinproteïen 1 (MeCP1), wat ’n hoë affiniteit vir ’n aantal gemetileerde CpG’s in ’n CGI het en dus digtheidspesifiek is. Die binding van MeCP1 aan die DNA verhoed sodoende direk die binding van TF’s (Singal en Grinder 1999). In teenstelling met MeCP1 kan metielsitosien-bindingsdomeinproteïen 2 (MeCP2) ook aan ’n enkele gemetileerde CpG-dinukleotied bind (lokus-spesifiek). MeCP2 werf op sy beurt ’n kompleks van onderdrukkers wat die binding van TF’s verhoed of die onderliggende chromatienstrukture verander en sodoende geendemping veroorsaak (Singal en Ginder 1999).
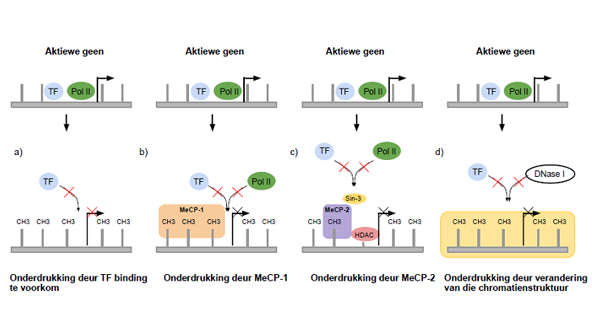
Figuur 2. Meganismes van geenonderdrukking deur DNA-metilering. (a) DNA-metilering in die bindingsetels van transkripsiefaktore (TF’s) kan geenuitdrukking direk inhibeer deur te verhoed dat hierdie TF’s en die polimerase II-ensiem (Pol II) aan die DNA-volgorde bind. (b) Digtheidspesifieke metilering kan geenuitdrukking direk inhibeer deur onderdrukkende metiel-bindende proteïene (MeCP1) te werf. (c) Lokus- en digtheidspesifieke metilering kan die uitdrukking van gene voorkom deur middel van metiel-bindende proteïen, MeCP2. Die MeCP2-kompleks bevat ensieme soos histoon-deasetilase (HDAC) wat die chromatienstruktuur verander en só op ’n indirekte wyse die binding van transkripsiefaktore voorkom. (d) Verder voorkom die veranderde chromatienstruktuur en hoë konsentrasie metielgroepe die toegang van DNase I tot die DNA en verlaag dus DNase I-sensitiwiteit. (Gebaseer op Singal en Ginder 1999)
2.2 Histoonmodifikasies
Spesifieke modifisering van histone vorm die tweede meganisme van epigenetiese modifikasies. Histone is klein, hoogs basiese kernproteïene. Twee kopieë van elk van die histone H2A, H2B, H3 en H4 assosieer in ’n histoonoktameer waarrondom ongeveer 147 basispare DNA gedraai is. Die kompleks van die histoonoktameer en ongeveer twee superheliese DNA-draaie (waarin sowat 147 basispare DNA vervat is) staan bekend as ’n nukleosoom en is die fondament van eukariotiese DNA-verpakking. Die inligting in DNA wat só verpak is, is bykans ontoeganklik weens die steriese hindernis wat dit tot die ensieme van informasiemetabolisme bied. Histone speel dus ’n belangrike rol in die kondensering van DNA, en die noue verwantskap tussen histone en DNA lei daartoe dat histoonmodifikasies byna elke aspek van DNA-verpakking en -funksie beïnvloed. Histoonmodifikasies word gekenmerk deur komplekse en diverse chemiese veranderings met die algemene neiging om te reageer op genomiese funksies en sluit asetilering, metilering, fosforilering, en ubikwitinering van die histone in (Nightingale et al. 2007). Hierdie modifikasies vind meestal op die ongestruktureerde, N-terminale domeine van die histone plaas en word bewerkstellig deur spesifieke ensieme. Die meganismes waardeur histoonmodifikasies geenuitdrukking beïnvloed, hou verband met ’n meegaande verandering van die chromatienstruktuur, hetsy direk of indirek. Histoonasetilering verwyder byvoorbeeld die positiewe lading op die histone en belemmer dus direk die histoon-DNA-interaksies wat tot kompakte chromatienstrukture lei. Gene wat geassosieer is met geasetileerde histone is dus losweg verpak en toeganklik vir die transkripsie-masjinerie. Hierteenoor word ’n di- of trimetielgroep op lisien 9 van histoon H3 (H3K9) byvoorbeeld deur die bindingsmodule heterochromatien proteïen 1 (HP1) herken. Naasliggende HP1-proteïene polimeriseer dan om digverpakte, onaktiewe chromatienvesels te vorm. Alhoewel die metilering van H3 dus nie ’n direkte invloed op die DNA-histoon-interaksie het nie, word geen-uitdrukking indirek beïnvloed. Só dien histoonmodifikasies dus as “merkers” vir latere prosesse wat geenregulering positief of negatief kan beïnvloed. Aangesien die bindingsmodules histoon-“merke” spesifiek herken, kodeer spesifieke histoonmodifikasies binne die konteks van ’n verpakte geen dus die uitdrukbaarheid van daardie geen. ’n Gedetailleerde bespreking van hierdie “histoon-kode” val buite die omvang van hierdie artikel; nietemin word die belangrikste geïdentifiseerde histoonmodifikasies en die biologiese konteks van elk in Tabel 1 saamgevat.
Tabel 1. Belangrike histoonmodifikasies en epigenetiese konteks van elk
| Histoon | Tipe modifikasie | Epigenetiese konteks |
|
Histoon H1 |
Fosforilering
Ubikwitinering |
Chromatien-kondensering, geen-spesifieke aktivering en onderdrukking. Transkripsie-aktivering. |
|
Histoon H2A |
Asetilering Ubikwitinering (H2-K123) |
Tetrahymena-oorlewing bepaal deur H2A-asetilering. |
|
Histoon H2B |
Ubikwitinering |
Voorvereiste vir H3 metilering. |
|
Histoon H3 |
Ubikwitinering Metilering (H3-K4, R17) |
Losmaak van nukleosoom. |
|
Histoon H4 |
Asetilering |
Transkripsie-aktivering. |
2.3 RNA-regulering
Ongeveer 98% van die sogenaamde “onsin”-DNA kodeer vir nikoderende RNA (ncRNA) van verskillende lengtes, soos opgesom in Tabel 2. ncRNA is alle funksionele RNA wat nie na proteïene vertaal word nie. Voorbeelde sluit in: die algemeen-bekende ncRNA, ribosomale RNA (rRNA) en oordrag-RNA (tRNA); kort ncRNA, waaronder mikro-RNA (miRNA), klein demper-RNA (siRNA) en piwi-wisselwerkende RNA (piRNA); gemiddelde lengte ncRNA, waaronder klein nukleolêre RNA (snoRNA); langer ncRNA, waaronder groot intrageniese ncRNA (lincRNA), vertaalde ultrabewaarde areas (T-UCR), en lang niekoderende RNA (lnRNA). ncRNA is ’n sleutel element van sellulêre homeostase en vorm die basis van RNA-regulering, die derde meganisme betrokke by epigenetiese modifikasies (Morris 2009). Verskeie ncRNA-molekules reguleer die uitdrukking en stabiliteit van gene in beide pro- en eukariote (Mattick en Makunin 2006). Regulering van geenuitdrukking vind plaas in trans en in cis. Rakende transkripsie en RNA-regulering word ’n trans-werkende element beskryf as DNA wat kodeer vir ’n ncRNA wat die transkripsie van ’n ander geen reguleer, terwyl ’n cis-werkende element verwys na ’n DNA-volgorde wat deur middel van TF’s en/of ander trans-werkende elemente die uitdrukking van gene op dieselfde chromosoom reguleer. Die meer bekende tRNA en rRNA vorm deel van die ncRNA-groep wat die translasie van boodskapper-RNA (mRNA) na proteïene bewerkstellig, terwyl die meerderheid van die ander ncRNA funksioneer om geenuitdrukking te voorkom (Mattick en Makunin 2006). ncRNA vorm deel van die RNA-induserende demperkompleks (RIDK). Spesifieke en minder spesifieke komplementêre basis-paring tussen dié ncRNA-volgordes en ander RNA-volgordes (boodskapper-RNA, mRNA) of DNA-volgordes lei tot die splitsing van die teiken-nukleotied-ketting soos voorgestel in Figuur 3 (Saxena et al. 2003).
Tabel 2. Tipes niekoderende RNA en hul onderskeie funksies
| Tipe ncRNA | Funksie | Grootte/Lengte |
|
Algemeen- bekende ncRNA |
|
|
|
rRNA |
Strukturele en ensiematiese komponente van die ribosome, die liggaampies waar proteïensintese plaasvind. Die ensiematiese werking van rRNA voorsien die meganisme vir proteïensintese deur hul interaksie met tRNA en mRNA. |
18 S – 1.9 kb |
|
tRNA |
Bind kovalent aan aminosure en bewerkstellig die aaneenskakeling van die groeiende proteïenketting. |
54 – 100 nt |
|
Kort ncRNA |
|
|
|
miRNA |
Onderdruk mRNA-translasie deur niespesifieke basis-paring tussen miRNA en teiken-mRNA. |
20-25 nt |
|
siRNA |
Onderdruk mRNA-translasie deur spesifieke basis-paring tussen siRNA en teiken-mRNA. |
20-25 nt |
|
tiRNA |
Mag ’n rol speel in die regulering van transkripsie. |
17-18 nt |
|
piRNA |
Vorm RNA-proteïen-komplekse deur die wisselwerking met piwi-proteïene om geendemping van retrotransposons te veroorsaak. |
26-31 nt |
|
Gemiddelde ncRNA |
|
|
|
snoRNA |
Voer lokus-spesifieke modifisering van nukleotiede in teiken-RNA (rRNA en mRNA) aan deur basis-paring tussen die snoRNA en die teiken-RNA. |
60-300 nt |
|
pRNA |
’n Groep lang en kort ncRNA wat geen-uitdrukking reguleer by promotors en transkripsie-beginpunte. |
22-200 nt |
|
TSSa-RNAs |
Mag ’n rol speel in die onderhoud van transkripsie. |
20-90 nt |
|
PROMPTs |
Mag ’n rol speel in die aktivering van transkripsie. |
<200 nt |
|
Lang ncRNA |
|
|
|
lincRNA |
Assosieer met chromatien-modifiserende komplekse om geenuitdrukking te bewerk. |
>200 nt |
|
T-UCR |
Mag ’n rol speel in die regulering van miRNA- en mRNA-vlakke. |
>200 nt |
|
TERRAs |
Onderhou die integriteit van telomeriese heterochromatien deur regulering van telomerase-aktiwiteit. |
>200 nt |
|
Ander lncRNA |
Speel ’n rol in X-chromosoom-onderdrukking en inprenting. |
>200 nt |

Figuur 3. RNA-demper-meganisme. LnRNA- en miRNA-voorlopers word in soogdiere verwerk tot siRNA- of miRNA-duplekse deur die Kapper-ensiem. Vervolgens word hierdie kort dubbeldraad-RNA-molekules afgedraai en ingebou in effektorkomplekse, naamlik RNA-induserende demperkompleks (RISC) en miRNA-bevattende effektorkompleks (miRNP). RIDC en miRNP bewerk afsonderlik afbraak en translasie-onderdrukking van teiken-mRNA. In soogdiere lei siRNA tot die splitsing van komplementêre teiken-RNA, terwyl die miRNA meestal betrokke is by die translasie-onderdrukking van teiken-mRNA. (Gebaseer op Meister en Tuschl 2004)
2.4 Proteïenkonformasieveranderinge
Meer onlangs is prions as ’n proteïenverwante epigenetiese meganisme geïdentifiseer in bakkersgis wat bydra tot oorerwing van omgewingsverworwe eienskappe (Halfmann en Lindquist 2010). Prions is ’n groep proteïene met ’n unieke vermoë om in ’n alternatiewe konformasie (konformeer) te vou as hul normale, nieprion-konformasie. Die veranderde konformasie van die prion het ’n direkte impak op proteïenfunksie. Skielike veranderinge in temperatuur, pH en intrasellulêre metaboliete hou onmiddellike gevolge in vir proteïenvouing en speel dus ’n belangrike rol in die induksie van prions, hul alternatiewe konformasie en funksie. Die abnormale proteïen-konformasie (prion-konformasie) plant voort deur homself af te druk op ’n homoloë proteïen. Prions kapitaliseer op die finale stap in die dekodering van die genetiese boodskap, naamlik proteïenvouing, om fenotipe-variasie teweeg te bring. Prions is stabiel tydens paring en meiose en word so na dogterselle oorgedra om stres-geïnduseerde verworwe eienskappe aan die nageslag oor te dra. Hierdie oorerflike omgewingsgeïnduseerde verandering steun die rol van proteïenvouing in epigenetika.
Prions is meer bekend vir malkoei- en Creutzfeldt-Jakob-siekte, maar prionproduksie in Sacchromyces ceriviciae bevoordeel oorlewing en aanwas tydens omgewingstres, is oorerflik en omkeerbaar (Halfmann en Lindquist 2010). Gedurende tye van omgewingstres vorm S. ceriviciae prions wat aanpassing by die omgewing steun en lei tot ’n verbeterde, sterker fenotipe. Kennis aangaande die positiewe rol van prions in die soogdier as gasheer is beperk. Voorlopige resultate op S. ceriviciae impliseer dat hierdie epigenetiese verskynsel ook ’n rol mag speel in die aanpassing van die mens by sy ewig veranderende omgewing.
2.5 Onderlinge afhanklikheid
Epigenetiese meganismes is verantwoordelik vir die toepassing en handhawing van patrone van geenuitdrukking wat seldifferensiasie in hoër eukariote meebring (Turner 2007). Epigenetiese meganismes werk nie in isolasie nie en verskeie epigenetiese merkers word gebruik om sellulêre seine op chromatienvlak te integreer. Verskeie modifikasies op histone en niehistoon-proteïene soos HMGs en DNA werk saam om chromatienveranderings te reguleer (Nightingale et al. 2007). MeCP-2-binding aan gemetileerde CpG-dinukleotiede veroorsaak byvoorbeeld nie net demping van geenuitdrukking deur die binding van TF’s te voorkom nie, maar ook deur die verandering in chromatienstruktuur as gevolg van histoon-deasetilering. Fuks et al. (2003) het getoon dat daar ook ’n verwantskap is tussen die metilering van lisien 9 op histoon 3 en DNA-metilering. Spesifieke komponente van die piRNA-sisteem is noodsaaklik om de novo metilering op die muis Rasgrf1-lokus te bewerkstellig en daarmee ’n betekenisvolle rol te speel by inprenting by dié lokus (Watanabe et al. 2011). Verder het dit ook onlangs bekend geword dat die regulering van DNMT’s bewerk word deur ncRNA. Regulering van metilering is dus afhanklik van die dinamiese interaksies tussen posttranslasionele modifikasies op DNMT’s en posttranskripsionele regulering deur miRNA. Alhoewel dit reeds bekend is dat vele ander ncRNA’s in wisselwerking met soogdier-DNMT’s is, is die presiese rol in die beheer van DNMT’s nog nie bekend nie (Dennis et al. 2011). Nietemin is dit duidelik dat ten minste nukleïensuurverwante epigenetiese meganismes in ’n streng-gereguleerde, noue verwantskap met mekaar funksioneer.
3. Epigenetiese oorerflikheid
Die epigenoom is besonder vatbaar vir veranderinge gedurende bevrugting en swangerskap, rondom geboorte en gedurende puberteit. Omgewingsfaktore wat epigenetiese veranderinge vroeg in die leeftyd van ’n individu induseer, kan die gesondheid van dié individu gedurende volwassenheid beïnvloed. Verhoogde vatbaarheid vir epigenetiese veranderinge tydens vroeë embrioniese fases hou moontlik verband met hoë vlakke van verskeie reguleerders van DNA-metilering en chromatienmodifikasie in embrionale stamselle en kiemselle (Feil en Fraga 2012). Transgenerasie epigenetiese oorerflikheid beskryf die oordrag van epigenetiese merke van ouer na kind tydens meiose (Skinner 2010). Blootstelling aan omgewingsfaktore gedurende gametogenese wat ’n verandering aan die epigenoom meebring, sal dus oorgedra word na die volgende generasie deur middel van transgenerasie epigenetiese oorerflikheid. Slegs merke wat oorgedra word na die F3-generasie is werklik transgeneratief, aangesien in utero-blootstelling eintlik die moeder (F0), die fetus (F1) en die primordiale kiemselle in die fetus (F2) beïnvloed. Mitotiese epigenetiese stabiliteit verseker die behoud van epigenetiese merke met DNA-replisering in somatiese selle tydens mitose (Skinner 2010). Dus bly die epigenetiese profiel relatief behoue gedurende die leeftyd van ’n individu, mits die omgewing konstant bly. Indien omgewingsfaktore wel die epigenoom van ’n spesifieke liggaamsel verander, word die veranderde epigenoom slegs oorgedra gedurende mitose en beïnvloed dus net dié selpopulasie van die individu. Veranderde epigenetiese merke in somatiese selle word nie oorgedra van een generasie na die volgende nie. Die finale epigenetiese profiel van ’n individu is dus die resultaat van beide mitotiese epigenetiese oorerflikheid en transgenerasie-oorerflikheid, waarvan beide gedeeltelik deur die omgewing beïnvloed word. Kennis van die regulering en oorerflikheid van epigenetiese merke is steeds beperk.
4. Moduleerders van epigenetika
Stogastiese veranderinge in die epigenoom word veroorsaak deur beide intrinsieke faktore en omgewingsfaktore. Intrinsieke faktore sluit alle geneties-bepaalde inherente faktore van ’n organisme in. Intrinsieke faktore soos volgorde-variasie is een manier waarop genetiese faktore as moduleerders van epigenetika kan optree. Volgorde-variasie kan direk en/of indirek bydra tot epigenetiese variasie. Polimorfismes in die DNA-volgorde kan byvoorbeeld direk daartoe lei dat CpG-dinukleotiede uit die genoom wegval of vorm en kan so potensieel die metileringsprofiel van ’n individu verander (Bjornson et al. 2004). Mutasies of polimorfismes in gene wat kodeer vir ensieme wat epigenetiese modifikasie reguleer, soos DNMT’s, metiel-bindende proteïene (MBP’s), en histoon- en ncRNA-moduleerders, kan op ’n indirekte wyse die epigenoom beïnvloed.
Die omgewing is ’n kragtige moduleerder van epigenetika. Navorsing toon dat die dieet van ouers ’n belangrike rol speel in die epigenoom-profiel van hul nageslag (Pembry et al. 2006). DNA- en histoon-metilering hang af van die vlakke van S-adenosielmetionien (SAM), die universele metiel-donor. SAM word vrygestel deur die metionien-siklus (ook bekend as die een-koolstof-siklus) in samewerking met die folaat-siklus (Figuur 4). ’n Dieet ryk aan metiel-donors kan DNA-metilering en gesondheid bevoordeel. Studies op Agouti-muise toon dat ’n metielryke dieet (cholien, foliensuur, vitamien B12 en betaïen) die pelskleur van afstammelinge verander en gesondheid bevoordeel deur die vlak van metilering van die agouti lang terminale herhaling (LTR) te verhoog (Cooney et al. 2002). Blootstelling van prenatale vroue aan diëtielstilbestrol, ’n sintetiese estrogeen, is geassosieer met epigenetiese veranderinge wat die kans op ginekologiese kankers verhoog (Li et al. 2003). Ongeag dieet kan die leefstyl van ’n ouer ook die epigenoom van ’n ongebore kind beïnvloed. Pembrey et al. (2006) het getoon dat tabakrook ’n paternale transgenerasie-effek op die liggaamsmassa-indeks van seuns het en dus as moduleerder van epigenetika optree. Alkoholgebruik deur vaders word ook geassosieer met die ontwikkeling van fetale alkoholspektrum-siektes as gevolg van verlaagde metilering by H19-DMR- en IG-DMR-gene in sperma-DNA (Ouko et al. 2009). Verder kan chemikalieë en besoedelingstowwe soos lugbesoedelingdeeltjies (Baccarelli et al. 2009), asbes (Christensen et al. 2009), silika (Umemera et al. 2008), benseen (Bollati et al. 2007) en swaarmetale (Baccarelli en Bollati 2009) soos chroom, kadmium, arseen en kwik, DNA-metilering by spesifieke gene in die mens verander en tot siektevatbaarheid bydra. ’n Studie op muise deur Manikkam et al. (2012) toon aan dat plastiek, dioksien en vliegtuigbrandstof ’n transgenerasie-effek op die voortplantingvermoëns van muise het. Terwyl die vroulike muise in die F1-, F2- en F3-generasie ’n vroeë aanvang toon tot puberteit, was spermatogeniese apoptose in manlike muise aangetas.
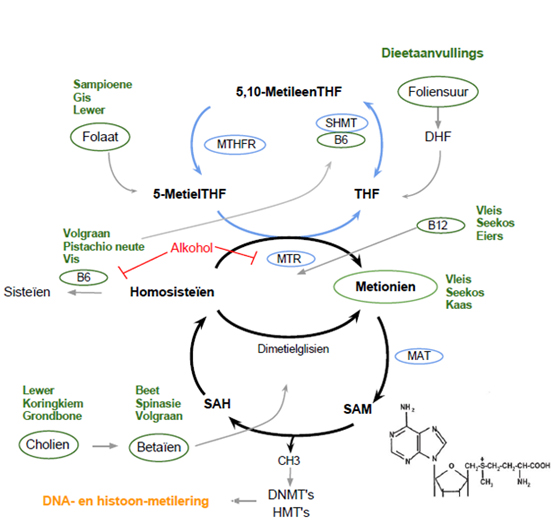
Figuur 4. Molekulêre meganismes wat omgewingsimpak bemiddel. Globale DNA- en histoon-metilering word beïnvloed deur liggaamsvlakke van S-adenosielmetionien (SAM). Intrasellulêre produksie van SAM is afhanklik van dieet of dieetaanvullings en word uitgevoer deur die metionien/1-koolstof-siklus (swart →). Gedurende dié siklus word metielgroepe vanaf die folaatsiklus (blou →) gebruik vir SAM-sintese. Folaat in die dieet en foliensuur in dieetaanvullings, dien as bron vir die folaatsiklus. Foliensuur word omskep in dihidrofolaat (DHF) voor dit as tetrahidrofolaat (THF) in die siklus geïnkorporeer word. Die folaatsiklus word gedryf deur die ensieme serien-hidroksimetieltransferase (SHMT), metileentetrahidrofolaat-reduktase (MTHFR) en 5-metieltetrahidrofolaat-homosisteïenmetieltransferase (MTR). Die metielgroepe wat vrygestel word deur die folaatsiklus word gebruik deur MTR om homosisteïen na metionien om te skakel. Metionien-adenosieltransferase (MAT) kataliseer die sintese van SAM vanaf metionien. SAM word omgeskakel na S-adenosielhomosisteïen (SAH) en vrygestelde metielgroepe word gebruik deur DNA- en histoonmetieltransferases (DNMT’s en HMT’s) om epigenetiese merke op DNA en histone aan te bring. Om die siklus te voltooi, word SAH gehidroliseer tot homosisteïen. Die metioniensiklus kan ook metielgroepe vanaf betaïen inlyf. Vitamiene B6 en B12 speel ’n belangrike rol in hierdie siklusse. B6 is betrokke by die omskakeling van homosisteïen na sisteïen, asook THF na 5,10-metileenTHF, terwyl B12 ’n kofaktor is vir MTR. Alkohol beïnvloed SAM-produksie negatief deur die omskakeling van homosisteïen na metionien en homosisteïen na sisteïen te inhibeer, laasgenoemde deur die vlakke van vitamien B6 te verander. (Gebaseer op Freil en Fraga 2012)
Die ingeprente epigenetiese merke wat die ouer se omgewingsfaktore weerspieël in die epigenoom van die afstammelinge is weer op hul beurt vatbaar vir moduleerders. Die epigenoom verander oor tyd. Byvoorbeeld, na bevrugting en die splitsing van die enkel sigoot waaruit ’n identiese (monosigotiese) tweeling ontwikkel, is die twee embrios se epigenoom, soos hul genoom, identies. Verskillende patrone van DNA-metilering en histoonasetilering word hierna neergelê, tensy hulle omgewing en leefstyl identies bly (Fraga et al. 2005). Die sielkundige omgewing gedurende vroeë ontwikkeling kan ook die epigenoom beïnvloed. McGowan et al. (2009) het getoon dat die promotors van glukokortikoïed-reseptore hipergemetileerd is in selfmoordgevalle waar die betrokke persone as kinders mishandel is.
Tesame met met die kumulatiewe effek van omgewingsfaktore oor tyd, speel ouderdom ook ’n rol in die modulering van epigenetika en studies het getoon dat die DNA-metilering voortdurend verander tydens ontwikkeling en veroudering. Takasugi (2011) het bevind dat die metileringsprofiel van 316 CpG-dinukleotiede in muise se spier-, brein- en lewerselle betekenisvol verskil tussen jong, volwasse en ou muise en dat die metilering in ou muise ooreenstem met die profiel van kankerselle en sekere siektetoestande. Verlaagde DNMT1-aktiwiteit en verhoogde uitdrukking van DNMT3, wat onderskeidelik globale hipometilering en hipermetilering by spesifieke CpG’s kataliseer (Lu et al. 2006), is voorgestel as moontlike faktore met ’n impak op die verouderende epigenoom (Zhang et al. 2002; Lu et al. 2006). Daar word dus afgelei dat daar ten spyte van akkumulerende omgewingsfaktore ook met die verloop van tyd ’n inherente afname in die funksie van regulatoriese ensieme is.
5. Epigenetika in gesondheid en siekte
Die verhouding tussen epigenoom, omgewing en siekte is kompleks en dit is onduidelik of die omgewing ’n direkte of indirekte impak op die epigenoom het. ’n Verdere onduidelikheid is of die klein veranderinge in die epigenoom die oorsaak of effek van siekte is. Nietemin, epigenetiese merke wat met siektes geassosieer word, kan gebruik word as biomerkers vir siekte-vatbaarheid indien dit teenwoordig is in die bestaande epigenoom, terwyl siekte-geïnduseerde epigenetiese veranderinge gebruik kan word om die erns en vordering van siekte, asook die effek van behandeling, te monitor. Huidige studies toon ’n groeiende lys siektetoestande met onderliggende epigenetiese meganismes (Tabel 3). ’n Duidelike illustrasie van oorerflike epigenetiese meganismes en siektes word gesien in kolonkanker, waar die DNA-wanparingsherstel-ensiem, gekodeer deur MLH1, onaktief is oor generasies heen van geaffekteerde individue as gevolg van DNA-metilering (Hitchins et al. 2007). Net soos regulering van geenuitdrukking deur epigenetiese meganismes van mekaar afhanklik is, is daar ook siektetoestande wat deur meer as een epigenetiese modifikasies beïnvloed word. Veelvuldige sklerose is een voorbeeld waar beide histoonmodifikasies en DNA-metilering ’n rol speel in die etiologie van die siekte. Chou et al. (2008) toon aan dat differensiële uitdrukking van HLA klas II-risiko-faktore vir veelvuldige sklerose deur verskeie histoonmodifikasies bewerk word. Huehn et al. (2009) wys weer op hulle beurt dat DNA-metilering FOXP3 geenuitdrukking demp en lei tot verlaagde uitdrukking van dié geen, verantwoordelik vir ’n proteïen betrokke by die ontwikkeling van regulatoriese T-selle. Die belang van die niekoderende genoom in siekte in die mens is grootliks bestudeer in die konteks van wydverspreide wanuitdrukking en -funksie van miRNA in kanker. Dit is nou duidelik dat ander tipes ncRNA ook ’n rol in kanker speel. Net so speel verskillende tipes ncRNA’n rol in ’n verskeidenheid niekanker-siektetoestande van onder andere neurologiese, kardiovaskulêre en ontwikkelingsaard. Esteller (2011) gee ’n volledige oorsig van die rol van ncRNA in siektes in die mens. Daar is groot belangstelling in terapeutiese strategieë om die wanuitdrukking en -funksie van ncRNA reg te stel.
Tabel 3. Siektetoestande bewerk deur spesifieke epigenetiese meganismes
| Siekte | Epigenetiese meganisme | Verwysing |
|
DNA-metilering |
|
|
|
Beckwith-Wiedemann-sindroom |
Mislukte DNA-metilering op die ncRNA-geen KCNQ1OT1. |
Weksberg et al. (2002) |
|
Outisme |
Differensiële uitdrukking van gene by chromosoom 7q word beheer deur maternale inprenting deur epigenetiese meganismes. |
Shannen (2006) |
|
Major-psigose |
Differensiële uitdrukking van stres- geassosieerde gene en gene wat ’n rol speel in neurologiese ontwikkeling a.g.v. abnormale DNA-metilering. |
Mill et al. (2008) |
|
Immuun-gebrek, sentromeer- |
Mislukte DNA-metilering by verskeie gene betrokke by ontwikkeling en immunologie a.g.v. ’n funksionele mutasie in DNMT3b. |
Jin et al. (2008) |
|
Breekbare X-sindroom |
Uitgebreide herhaalde CGG-volgordes in die FMR1 5’ UTR-promotor-area word deur DNA-metilering gedemp. |
Oostra en Willemsen (2002) |
|
Vetsug |
Veranderde geenuitdrukking van ongeïdentifiseerde gene deur FTO- geenproduk, ’n DNA-demetilase. |
Gerkin et al. (2007) |
|
Histoonmodifikasies |
|
|
|
Asma |
Verlaagde histoon-deasetilase- en verhoogde histoon-asetieltransferase- aktiwiteit verminder NF-κB-inhibisie. |
Adcock et al. (2005) |
|
Kroniese obstruktiewe pulmonêre siekte |
Verlaagde histoon-deasetilase-aktiwiteit verminder NF-κB-inhibisie deur verhoogde histoon-asetilering. |
Adcock et al. (2005) |
|
Leukemie |
Chromosomale translokasie deur histoon-asetieltransferase en -metieltransferase. |
Claus en Lubbert (2003) |
|
Niekoderende RNA |
|
|
|
Alzheimer se siekte |
Verhoogde vlakke van die niekoderende anti-sin transkrip vir beta-sekretase-1 (BACE1), BACE1-AS, korreleer met amiloïed-β1-42, wat in verhoogde vlakke voorkom in Alzheimer-pasiënte. |
Faghihi et al. (2008) |
|
Parkinson se siekte |
Genetiese variasie in die FGF20-geen beïnvloed die binding van miRNA-433 en bevorder die uitdrukking van FGF20 wat lei tot verhoogde vlakke α-sinukleïen. |
Wang et al. (2008) |
Die toenemende belangstelling in die rol van epigenetika in siekte-ontwikkeling mag voordele inhou, aangesien epigenetiese afwykings, in teenstelling met geenmutasies, deur natuurlike of sintetiese epifarmaseutiese middels herstel kan word (Peedicayil 2008). Dus kan spesifieke moduleerders van die epigenoom gebruik word om afwykings te herstel. Huidige navorsing op epigenetiese terapie is grootliks gemik op kanker, aangesien die rol van epigenetika tot dusver die beste verstaan word in kanker. Die DNA-metilase-onderdrukker 5-aza-2-deoksisitidien is reeds in 2006 deur die derde fase van kliniese toetse vir die behandeling van akute miëloïed-leukemie, waarna dit deur die FDA aanvaar is (Boumber en Issa 2011). Kliniese toetse word tans uitgevoer op ander chemiese middels wat die potensiaal het om epigenetiese afwykings in verskeie kankers om te keer. Hierdie epifarmaseutiese middels is merendeels gemik op histoonmodifikasies en DNA-metilering, aangesien ’n spesifieke ncRNA gewoonlik die uitdrukking van meer as een geen reguleer en die teikening daarvan wyer implikasies het en newe-effekte mag inhou. ’n Nadeel van middels wat metilering globaal beïnvloed, is dat dit nie spesifiek is nie, en alhoewel dit voordelig is om byvoorbeeld onkogene te onderdruk deur verhoogde DNA-metilering, kan genoom-wye hipermetilering weer op sy beurt nadele tot gevolg hê. Dus lê daar nog baie werk voor om epigenetiese terapie meer spesifiek te maak.
6. Metodes vir die bestudering van epigenetika
6.1 DNA-metilering
Dit is byna onmoontlik om DNA-metilering by ’n spesifieke lokus te bestudeer sonder voorafgaande metilering-afhanklike behandelings. Die drie basiese metilering-afhanklike behandelings sluit in: restriksie-ensieme, affiniteitsverryking en natriumbisulfaat-omskakeling. ’n Wye verskeidenheid molekulêre biologiese tegnieke, soos die polimerase-kettingreaksie (PCR), hibridisering- en volgordebepalingmetodes word gebruik om 5mC-nukleotiede op te spoor nadat die genomiese DNA op een van bogenoemde maniere behandel is. Die kombinasie van die verskillende voorafgaande behandelings en daaropvolgende analitiese tegnieke het daartoe gelei dat daar vandag ’n groot verskeidenheid tegnieke is om hierdie epigenetiese modifikasie te bestudeer (Laird 2010). Die meerderheid van hierdie tegnieke is gemik op die bestudering van metilering op genoom-wye en lokus-spesifieke vlak. Natriumbisulfaat-omskakeling gevolg deur volgordebepaling is die norm en alle metileringspatrone behoort met hierdie behandeling bevestig te word (Laird 2010). Natriumbisulfaat-behandeling verander alle ongemetileerde sitosienbasisse na tiamien en sodoende kan metilering by spesifieke CpG-dinukleotiede opgespoor word en gekwantifiseer word deur ’n volgordebepaler.
Tegnieke wat gebruik maak van die polimerase-kettingreaksiemetode kan verder in twee subklasse verdeel word op grond van die inleier wat gebruik word. Die een groep gebruik inleiers wat spesifiek gemetileerde (of ongemetileerde) template amplifiseer, byvoorbeeld metilering-spesifieke PCR (MSP). Die tweede groep gebruik inleiers wat die templaat sal amplifiseer ongeag die metileringsprofiel, byvoorbeeld natriumbisulfaat-volgordebepaling, restriksie-ensiem-vertering en smeltkurwe-analises. Tabel 4 gee ’n oorsig van die mees algemene tegnieke vir die bestudering van DNA-metilering.
Tabel 4. Metodes vir die bestudering van DNA-metilering
| Tegniek | Beginsel | Voordele | Nadele |
|
Metilering-sensitiewe enkelstring- konformasie-analise |
Natriumbisulfaat-behandeling verander die primêre en so die sekondêre struktuur van enkelstring-DNA. Metileringsdigtheid word bepaal deur veranderde mobiliteit gedurende elektroforese. |
Ekonomies en sensitief by hoër persentasies metilering. |
Lae sensitiwiteit by laer metileringsdigthede. Onvoltooide bisulfaat-omskakeling kan vals negatiewe resultate lewer. |
|
Gemetileerde DNA- immunopresipitasie gekoppel aan DNA-mikromatriks |
Gebruik teenliggame gerig teen 5mC gevolg deur immunopresipitasie en hibridisering op ’n DNA-mikromatriks. |
Onafhanklik van bisulfaat-omskakeling en ideaal vir genoom-wye analises. |
Duur. |
|
Metilering-sensitiewe restriksie-ensieme gevolg deur PCR |
Restriksie-ensieme word gebruik om die DNA te sny by gemetileerde óf ongemetileerde C-nukleotiede. PCR sal die produk slegs in die afwesigheid van splitsing amplifiseer. |
Ekonomies en tydbesparend. |
Metileringstudies is beperk tot DNA-volgordes wat herken word deur die restriksie-ensieme. |
|
Gekombineerde bisulfaat- en restriksie-ensiem-analise |
Natriumbisulfaat-omskakeling word gevolg deur PCR wat die hele volgorde van belang amplifiseer. Restriksie-ensieme word gebruik om by CpG-dinukleotiede te sny voordat densitometrie gebruik word om die hoeveelheid splitsing te bepaal. |
Beter sensitiwiteit in vergelyking met ander restriksie-ensiem-tegnieke. |
Intensiewe tegniek wat beperk is tot DNA-volgordes wat herken word deur die restriksie-ensieme. |
|
Metilering-spesifieke hoë- resolusie- smeltkurwe-analise |
Natriumbisulfaat-omskakeling word gevolg deur kwantitatiewe PCR, waarna die smeltkurwes ontleed word deur hoë-resolusie-smeltkurwe-sagteware. Sitosien bly behoue tydens omskakeling indien gemetileerd. Meer sitosien-guanien-basis-pare smelt by ’n hoër temperatuur. |
Sensitief en tydbesparend. |
Duur. |
|
Volgordebepaling deur sintese |
Natriumbisulfaat-omskakeling gevolg deur volgordebepaling gee die metileringsprofiel by ’n spesifieke CpG-dinukleotied. |
Sensitief en tydbesparend. |
Afhanklik van absolute omskakeling deur natriumbisulfaat. |
a Algemene Engelse afkortings vir tegnieke.
6.2 Histoonmodifikasies
Kennis aangaande die histoonmodifikasies oor ’n spesifieke geen (of regulatoriese element) is noodsaaklik om die epigenetiese konteks rondom geenuitdrukking te verstaan. Chromatien-immunopresipitasie (ChIP) word algemeen vir hierdie doel ingespan. Die standaard ChIP-toepassing begin met die isolasie van selkerne waarna kernproteïene geëkstraheer en kovalent aan DNA gekruiskoppel word (dikwels d.m.v. formaldehied). Ná kernlise word die chromatien gefragmenteer met sonikasie of ensiematiese vertering en korter chromatien-fragmente word gepresipiteer deur ’n teenliggaam gerig teen die spesifieke histoonmodifikasie. Chromatienfragmente wat nie die betrokke modifikasie bevat nie, bly dus in oplossing. Hierna word die DNA uit die presipitaat gesuiwer vir verdere analises. Die polimerase-kettingreaksie (PCR) en kwantitatiewe PCR (qPCR) kan gebruik word om te bepaal of ’n spesifieke DNA-volgorde met die betrokke histoonmodifikasie geassosieer was (ChIP-PCR). Dit is egter ook moontlik om die assosiasie van ’n spesifieke histoonmodifikasie genoom-wyd vas te stel deur die gesuiwerde DNA op ’n mikromatriks te hibridiseer (“ChIP-on-Chip”). Die mees moderne benadering is egter om die gesuiwerde DNA se basisvolgorde te bepaal deur middel van volgordebepaling deur sintese (“ChIP-Seq”). Deur die aanvanklike immunopresipitasie met teenliggame teen verskillende gemodifiseerde histone uit te voer, kan daar dus bepaal word of ’n reeks modifikasies by ’n spesifieke lokus aangetref word.
In sommige gevalle is dit egter nuttig om globale (genoom-wye) veranderinge in histoonmodifikasies te bepaal sonder dat die lokaliteit van die modifikasies in ag geneem word. Hier speel hoë-resolusie-massaspektrometrie ’n sleutelrol. Histone wat uit selle of weefsels geëkstraheer is, word tipies geskei d.m.v. poliakrielamied-jel-elektroforese (PAGE) en dan in die jel deur ensieme verteer tot kleiner peptiede. Histoonpeptiede wat ’n betrokke modifikasie bevat, kan dan verryk word deur middel van ’n breë spektrum van metodes. Die verrykte monster word vervolgens op ’n mikrokolom (dikwels binne die konteks van hoëverrigting-vloeistofchromatografie (HPLC) of ultraverrigting-vloeistofchromatografie (UPLC) geskei en deur middel van elektrosproei-ionisering voorberei vir analise deur massaspektroskopie (MS). In ’n tandem MS (MS2)-eksperiment word ’n spesifieke peptiedioon deur die eerste MS geselekteer op grond van ’n kenmerkende massa-tot-lading-verhouding (m/z) en deurgevoer na ’n botsing-sel waar dit gefragmenteer word om die aminosuurvolgorde van die peptied in die tweede MS te bepaal. In die geval van peptiede wat posttranslasioneel gemodifiseer is, sal die teenwoordigheid van ’n modifikasie gereflekteer word in ’n massaverskuiwing wat ooreenstem met die massa van die modifikasie. Dit is dus moontlik om die presiese posisie van modifikasie te bepaal. Met behulp van die massawaardes wat in bogenoemde analises opgelewer word, word proteïene geïdentifiseer uit aanlyn-databasissoektogte. Wat bogenoemde metodes gemeen het, is dat histoonmodifikasies in vivo bestudeer word. Vanuit ’n molekulêr-epigenetika-oogpunt, is dit egter soms nodig om in vitro-eksperimente uit te voer om die ensieme wat posttranslasionele modifikasies aanbring, sowel as die spesifieke betrokke aminosuurresidue te identifiseer.
6.3 Niekoderende RNA
Die kwantitatiewe analises van klein ncRNA van kort of gemiddelde lengte, soos miRNA, siRNA, piRNA, en snoRNA, word gekompliseer deur die klein grootte van hierdie molekules. RNA-kladtegniek is die standaardmetode vir die identifikasie en kwantifisering van RNA, maar vereis ’n betreklik groot hoeveelheid beginmateriaal van 10-20 µg totale RNA of meer as 5 µg klein ncRNA (Ro en Yan 2010). Die tegniek is tyd- en arbeidsintensief en maak gebruik van radioaktiewe isotope. ’n Tweede tegniek maak staat op ’n tipe PCR waar geïsoleerde klein ncRNA in ’n ensiematiese reaksie poli(A)-sterte kry aan die 3’-kant van die volgorde deur poliadenilering. snoRNA-komplementêre-DNA (cDNA) word dan gesintetiseer deur trutranskripsie en ’n inleier wat bestaan uit ’n passtuk aan die 5’-kant en ’n poli(T)-stert aan die 3’-kant. Kwantitatiewe PCR en/of konvensionele PCR kan dan uitgevoer word deur ’n inleier te gebruik wat spesifiek gerig is tot die klein ncRNA wat van belang is en die universele inleier met die passtuk en poli(T)-stert (Ro en Yan 2010).
Ander ncRNA word dikwels ondersoek met behulp van cDNA-biblioteke en die nuwe generasie volgordebepalingstegnieke. Alhoewel volgordebepalingstegnieke die ondersoeker toegang gee tot byna elke tipe ncRNA in ’n organisme, moet spesifieke funksies en uitdrukkingspatrone met behulp van PCR in spesifieke selle bevestig word. Mikromatrikse vir reeds bevestigde ncRNA is kommersieel beskikbaar en word aanbeveel vir spoedige genoom-wye analises van ’n groot aantal monsters. Mikromatriks-analises is akkuraat en tydbesparend, maar is beperk tot bekende ncRNA-molekules.
7. Samevatting
Genetiese volgorde tesame met epigenetiese variasie bepaal fenotipe. Normale veranderinge aan die epigenetiese profiel staan sentraal in ontwikkelingsbiologie, terwyl nadelige epigenetiese variasie bydra tot die vatbaarheid en ontwikkeling van siektes. Begrip van die rol van DNA-metilering, histoonmodifikasies en ncRNA in geenregulering het gegroei, maar kennis oor die regulering en oorerflikheid daarvan is steeds beperk. Epigenetika hou implikasies in vir sel-, evolusie- en mediese biologie. Daar is toenemend waardering vir die belang van epigenetika in siekte en gesondheid. Die gebruik van epifarmaseutiese middels in kanker illustreer die omkeerbaarheid van nadelige epigenetiese variasie en moedig die ontwikkeling van die epifarmaseutiese bedryf aan. Navorsing op epigenetika kan lei tot ’n beter begrip van die patogenese van siektes en kan ook lig werp op die verskille in siektevatbaarheid tussen populasies en die impak van die omgewing op die verskynsel. Epigenetika mag belangrike implikasies inhou vir siektes wat deur ’n verarmde omgewing beïnvloed word en wat algemeen in sub-Sahara-Afrika voorkom, soos tuberkulose, MIV/VIGS en malaria.
Erkenning
Die outeurs bedank prof. Ian Dubery vir aanmoediging om in ons moedertaal te publiseer. Ons navorsing word gesteun deur die NRF, WNNR en CANSA.
Bibliografie
Avery, O.T., C.M. MacLeod, M. McCarty. (1944) Studies on the chemical nature of the substance inducing transformation of pneumococcal types induction of transformation by a desoxyribonucleic acid fraction isolated from pneumococcus type iii, J Exp Med. 79(2): 137-58.
Adcock, I.M., K. Ito, P.J. Barnes. (2005) Histone deacetylation: an important mechanism in in?ammatory lung diseases, COPD 2(4): 445-55.
Baccarelli, A., V. Bollati. (2009) Epigenetics and environmental chemicals, Current Opinion in Pedeatrics. 21(2): 243-51.
Baccarelli, A., R.O. Wright, V. Bollati, L. Tarantini, A.A. Litonjua, H.H. Suh, A. Zanobetti, D. Sparrow, P.S. Vokonas, J. Schwartz. (2009) Rapid DNA methylation changes after exposure to traffic particles, American Journal of Respiratory and Critical Care Medicine. 179(7): 572-578.
Bollati, V, A. Baccarelli, L. Hou, M. Bonzini, S.Fustinoni, D. Cavallo, H.M. Byun, J. Jiang, B. Marinelli, A.C. Pesatori, P.A. Bertazzi, A.S. Yang. (2007) Changes in DNA methylation patterns in subjects exposed to low-dose benzene, Cancer Research. 67 (3):876-80.
Boumber,Y., J.P. Issa. (2011) Epigenetics in cancer: What's the future? Oncology. 25 (3): 220-8.
Boyes, J., A. Bird. (1991) DNA methylation inhibits transcription indirectly via a methyl-CpG binding protein, Cell. 64 (6): 1123-34.
Christensen, B.C., E.A. Houseman, C.J. Marsit, S. Zheng, M.R. Wrensch, J.L. Wiemels, H.H. Nelson, M.R. Karagas, J.F. Padbury, R. Bueno, D.J. Sugarbaker, R.F. Yeh, J.K. Wiencke, K.T. Kelsey. (2009) Aging and environmental exposures alter tissue-specific DNA methylation dependent upon CpG island context, PLoS Genet. 5(8):e1000602.
Chou, S.D., T.B. Tomasi. (2008) Spatial distribution of histone methylation during MHC class II expression, Mol Immunol. 45(4):971-80.
Claus, R., M. Lubbert. (2003) Epigenetic targets in hematopoietic malignancies, Oncogene. 22(42): 6489-96.
Cooney, C.A., A.A. Dave, G. Wolff. (2002) Maternal methyl supplements in mice affect epigenetic variation and DNA methylation of offspring, J Nutr. 132(8 Suppl):2393S-2400S.
Cubas, P., C. Vincent, E. Coen. (1999) An epigenetic mutation responsible for natural variation in floral symmetry, Nature. 401(6749):157-61.
Darwin, C. (1859) On the Origin of Species by Means of Natural Selection; or, The Preservation of Favoured Races in the Struggle for Life. London, uK: John Murray
Darwin, C. (1868) The Variation of Animals and Plants Under Domestication. London, UK: John Murray
Darwin, F. (ed) (1888) The Life and Letters of Charles Darwin. London, uK: John Murray
Dennis, H., M.N. Ndluvo, F. Fuks. (2011) Regulation of mammalian DNA methyltransferases: a route to new mechanisms, EMBO Rep. 12(7):647-56.
Esteller, M. (2011) Non-coding RNAs in human disease, Nat Rev Genet. 12(12):861-74.
Faghihi, M.A., F. Modarresi, A.M. Khalil, D.E. Wood, B.G.Sahagan, T.E. Morgan, C.E. Finch, G. St. Laurent III, P.J. Kenny, C. Wahlestedt. (2008) Expression of a noncoding RNA is elevated in Alzheimer's disease and drives rapid feed-forward regulation of β-secretase, Nat Med. 14(7):723-30.
Fraga, M.F., E. Ballestar, M.F. Paz, S. Ropero, F. Setien, M.L. Ballestar, D. Heine-Suñer, J.C. Cigudosa, M. Urioste, J. Benitez, M. Boix-Chornet, A. Sanchez-Aguilera, C. Ling, E. Carlsson, P. Poulsen, A. Vaag, Z. Stephan, T.D. Spector, Y.Z. Wu, C. Plass, M. Esteller. (2005) Epigenetic differences arise during the lifetime of monozygotic twins, Proc Natl Acad Sci U S A. 102(30):10604-9.
Feil, R., MF. Fraga. (2012) Epigenetics and the environment: emerging patterns and implications, Nat Rev Genet. 13(2):97-109.
Frith, M.C., M. Pheasant, J.S. Mattick. (2005) The amazing complexity of the human transcriptome, Eur J Hum Genet. 13(8):894-7.
Fuks, F., P.J. Hurd, R. Deplus, T.Kouzarides. (2003) The DNA methyltransferases associate with HP1 and the SUV39H1 histone methyltransferase, Nucleic Acids Res. 31(9):2305-12.
Gerken, T. C.A.Girard, Y.L. Tung, C.J.Webby, V. Saudek, K.S. Hewitson, G.S.H.Yeo, M.A. McDonough, S. Cunliffe, L.A. McNeill, J. Galvanovskis, P. Rorsman, P. Robins, X. Prieur, A.P. Coll, M. Ma, Z. Jovanovic, I.S.Farooqi, B.Sedgwick, I. Barroso, T. Lindahl, C.P. Ponting, F.M. Ashcroft, S.O'Rahilly, S.J. Schofield. (2007) The obesity-associated FTO gene encodes a 2-oxoglutarate-dependent nucleic acid demethylase, Science. 318(5855):1469-72.
Goll, M.G., T.H. Bestor. (2005) Eukaryotic cytosine methyltransferases, Annu Rev Biochem. 2005;74:481-514.
Halfmann, R., S. Lindquist. (2010) Epigenetics in the Extreme: Prions and the Inheritance of Environmentally Acquired Traits, Science 330(6004): 629-32.
Handel, A.E., G.C. Ebers, S.V. Ramagopalan. (2010) Epigenetics: molecular mechanisms and implications for disease, Trends Mol Med. 16(1):7-16.
Harvey, W. (1651) On the Generation of Animals (Exercitationes de Generatione Animalium) (“Experiments Concerning Animal Generation”). Canada, USA: ProQuest.
Hitchins, M.P., J.J. Wong, G. Suthers, C.M. Suter, D.I. Martin, N.J. Hawkins, R.L. Ward. (2007) Inheritance of a cancer-associated MLH1 germ-line epimutation, N Engl J Med. 356(7):697-705.
Huehn, J., J.K. Polansky, A. Hamann. (2009) Epigenetic control of FOXP3 expression: the key to a stable regulatory T-cell lineage? Nat Rev Immunol. 9(2):83-9.
Jin, B., Q. Tao, H.M. Soo, W. Wu, J. Ying, C.R. Fields, A.R. Delmas, X. Liu, J. Qiu, K.D. Robertson (2008) DNA methyltransferase 3B (DNMT3B) mutations in ICF syndrome lead to altered epigenetic modi?cations and aberrant expression of genes regulating development, neurogenesiss and immune function, Hum Mol Genet. 17(5):690-709.
Jones, P.A. S.B. Baylin. (2002) The fundamental role of epigenetic events in cancer. Nat Rev Genet. 3(6):415-28.
Jones,P.A., S.B. Baylin. (2007) The epigenomics of cancer. Cell. 128(4):683-92.
Klose, R.J., A.P. Bird. (2006) Genomic DNA methylation: The mark and its mediators, Trends Biochem Sci. 31(2):89-97
Krumlauf, R. (1996) Northern blot analysis, Basic DNA and RNA protocols, Methods in Molecular Biology, Volume 58. Humana Press Inc., Totowa, NJ.
Kucharski, R., J. Maleszka, S. Foret, R. Maleszka. (2008) Nutritional control of reproductive status in honeybees via DNA methylation, Science. 319(5871):1827-30.
Laird, P.W. (2010) Principles and challenges of genome-wide DNA methylation analysis, Nat Rev Genet. 11: 191-203.
Lamarck, J.B. (1809) Philosophie Zoologique. Paris, France: JB Baillière.
Lesk, A.M. (2008) Introduction to bioinformatics. UK: Oxford University Press.
Li, S., S.D. Hursting, B.J. Davis, J.A. McLachlan, J.C. Barrett. (2003) Environmental exposure, DNA methylation, and gene regulation: lessons from diethylstilbestrol-induced cancers, Ann N Y Acad Sci. 983:161-9.
Liu, Y., Y. Balaraman, G. Wang, K.P. Nephew, F.C. Zhou. (2009) Alcohol exposure alters DNA methylation profiles in mouse embryos at early neurulation. Epigenetics. 4(7):500-11.
Lu, Q., X. Qiu, N. Hu, H. Wen, Y. Su, B.C. Richardson. (2006) Epigenetics, disease, and therapeutic interventions, Ageing Res Rev. 5(4):449-67.
Luger, K., A.W. Mader, R.K. Richmond, D.F. Sargent, T.J. Richmond. (1997) Crystal structure of nucleosome core particles at 2.8A resolution, Nature. 389(6648):251-60.
Manikkam, M., C. Guerrero-Bosagna, R.Tracey, M.M. Haque, M.K. Skinner. (2012) Transgenerational Actions of Environmental Compounds on Reproductive Disease and Identification of Epigenetic Biomarkers of Ancestral Exposures, PLoS One. 7(2):e31901.
Mattick, J.S., I.V. Makunin. (2006) Non-coding RNA, Hum Mol Genet. 15 Spec No 1:R17-29.
McGowan, P.O., A. Sasaki, A.C. D'Alessio, S. Dymov, B. Labonté, M. Szyf, G. Turecki, M.J Meaney. (2009) Epigenetic regulation of the glucocorticoid receptor in human brain associates with childhoodabuse, Nat Neurosci. 12(3):342-8.
Mendel, G. (1866) Versuche über Pflanzen-Hybriden. New York, USA:Lubrecht & Cramer, Limited
Mill, J., T. Tang, Z. Kaminsky, T. Khare, S. Yazdanpanah, L. Bouchard, P. Jia, A. Assadzadeh, J. Flanagan, A. Schumacher, S.C. Wang, A. Petronis. (2008) Epigenomic pro?ling reveals DNA-methylation changes associated with major psychosis, Am J Hum Genet. 82(3):696-711.
Morris, K.V. (2009) Long antisense non-coding RNA function to direct epigenetic complexes that regulate transcription in human cells, Epigenetics. 4(5):296-301.
Ndlovu, M.N., H. Denis, F. Fuks. (2011) Exposing the DNA methylome iceberg, Trends Biochem Sci. 36(7):381-7.
Nightingale, K.P., L.P. O’Neill, B.M. Turner. (2006) Histone modi?cations: signalling receptors and potential elements of a heritable epigenetic code, Curr Opin Genet Dev. 16(2):125-36.
Oostra, B. A., R. Willemsen. (2002) The X chromosome and fragile X mental retardation, Cytogenet Genome Res. 99(1-4):257-64.
Ouko, L.A., K. Shantikumar, J. Knezovich, P. Haycock, D.J. Schnugh, M. Ramsay. (2009) Effect of alcohol consumption on CpG methylation in the differentially methylated regions of H19 and IG-DMR in male gametes: implications for fetal alcohol spectrum disorders, Alcohol Clin Exp Res. 33(9):1615-27
Peedicayil, J. (2008) Pharmacoepigenetics and pharmacoepigenomics, Pharmacogenomics. 9(12):1785-6.
Pembrey, M.E., L.O. Bygren, G. Kaati, S. Edvinsson, K. Northstone, M. Sjöström, J. Golding, ALSPAC Study Team. (2006) Sex-speci?c, male-line transgenerational responses in humans, Eur J Hum Genet. 14(2):159-66.
Ro, S., W. Yan. (2010) Detection and Quantitative Analysis of Small RNA by PCR, Methods Mol Biol. 629:295-305.
Saxena, S., Z.O. Jonnson, A. Dutta. (2003) Small RNA with Imperfect Match to Endogenous mRNA Repress Translation, J Biol Chem. 278(45):44312-9.
Schanen, N.C. (2006) Epigenetics of autism spectrum disorders, Hum MolGenet. 15 (Spec. No. 2), R138-R150.
Sigurdsson, M.I., A.V. Smith, H.T. Bjornsson, J.J. Jonsson. (2009) HapMap methylation-associated SNPs, markers of genrmline DNA methylation, positively correlate with regional levels of human meiotic recombination, Genome Res. 19(4):581-9.
Singal, R., G.D. Ginder. (1999) DNA methylation, Blood 93(12) 4059-70.
Skinner, M.K. (2011) Environmetal epigenomics and disease susceptibility, EMBO Rep. 12(7):620-2.
Spemann, H. (1938) Embryonic Development and Induction. New Haven, CT: Yale University Press.
Takasugi, M. (2011) Progressive age-dependent DNA methylation changes start before adulthood in mouse tissues, Mech Ageing Dev. 132(1-2):65-71.
Tate, P.H., A.P. Bird. (1993) Effects of DNA methylation on DNA-binding proteins and gene expression, Curr Opin Genet Dev. 3(2):226-31.
Turner, B.M. (2007) Defining an epigenetic code, Nat Cell Biol. 9(1):2-6.
Umemura, S., N. Fujimoto, A. Hiraki, K. Gemba, N. Takigawa, K. Fujiwara, M. Fujii, H. Umemura, M. Satoh, M. Tabata, H. Ueoka, K. Kiura, T. Kishimoto, M. Tanimoto. (2008) Aberrant promoter hypermethylation in serum DNA from patients with silicosis, Carcinogenesis. 29(9):1845-9.
Verhoeven, K.J. J.J.Jansen, P.J. van Dijk, A. Biere. (2010) Stress-induced DNA methylation changes and their heritability in asexual dandelions, New Phytol. 185(4):1108-18.
Waddington , C.H. (1942) The epigenotype, Endeavour. 1: 18-20.
Wang, G., J.M. van der Walt, G. Mayhew, Y.J. Li, S. Züchner, W.K. Scott, E.R. Martin, J.M. Vance. (2008) Variation in the miRNA-433 binding site of FGF20 confers risk for Parkinson disease by overexpression of alpha-synuclein, Am J Hum Genet. 82(2):283-9.
Watanabe, T., S. Tomizawa, K. Mitsuya, Y. Totoki, Y. Yamamoto, S. Kuramochi-Miyagawa, N. Iida, Y. Hoki, PJ. Murphy, A. Toyoda, K. Gotoh, H. Hiura, T. Arima, A. Fujiyama, T. Sado, T. Shibata, T. Nakano, H. Lin, K. Ichiyanagi, P.D. Soloway, H. Sasaki. (2011) Role for piRNA and Noncoding RNA in de Novo DNA Methylation of the Rasgrf1 Imprinted Mouse Locus, Science. 332(6031):848-52.
Watson, J.D., F.H.C. Crick. (1953) Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid. Nature 17: 737-738.
Weaver, I.C., N. Cervoni, F.A. Champagne, A.C. D'Alessio, S. Sharma, J.R. Seckl, S. Dymov, M.Szyf, M.J. Meaney. (2004) Epigenetic programming by maternal behavior, Nat Neurosci. 7(8):847-54.
Weismann, A. (1893) The Germ-Plasm: A Theory of Heredity. New York, USA: Charles Scribner’s Sons
Weismann, A. (1889) The supposed transmission of mutilations. In Essays upon Heredity and Kindred Problems, EB Poulton, S Schönland, AE Shipley (eds). Oxford, UK: Clarendon.
Weksberg, R., C. Shuman, O. Caluseriu, A.C. Smith, Y.L. Fei, J. Nishikawa, T.L. Stockley, L. Best, D. Chitayat, A. Olney, E. Ives, A.M. Schneider, T.H. Bestor, M. Li, P. Sadowski, J. Squire. (2002) Discordant KCNQ1OT1 imprinting in sets of monozygotic twins discordant for Beckwith-Wiedemann syndrome, Hum Mol Genet. 11(11):1317-25.
Yen, T.T., A.M. Gill, L.G. Frigeri, G.S. Barsh, G.L. Wolff. (1994) Obesity, diabetes, and neoplasia in yellow Avy/- mice: ectopic expression of the agouti gene, FASEB J. 8(8):479-88.
Young, E. (2008) Strange inheritance: Rewriting Darwin and Dawkins? In sickness and in health, New Scientist 12:29-33.
Zhang, Z., C. Deng, Q. Lu, B. Richardson, (2002) Age-dependent DNA methylation changes in ITGAL (CD11a) promoter, Mech Ageing Dev. 123(9):1257-68.

Ontvang: 28 Februarie 2012
Geplaas: 15 Augustus 2012

